Visão Geral da Divisão de Dispositivos Médicos (MDD) e do MDACS em Hong Kong
Uma visão geral da Divisão de Dispositivos Médicos (MDD) do Departamento de Saúde e do Sistema de Controle Administrativo de Dispositivos Médicos (MDACS) voluntário, que garante a segurança dos dispositivos em Hong Kong.
Visão geral
Resumo deste regulador ou jurisdição e sua relação com o acesso ao mercado.
Introdução
A Divisão de Dispositivos Médicos (MDD), subordinada ao Departamento de Saúde do Governo da Região Administrativa Especial de Hong Kong, é o órgão regulador responsável por supervisionar a segurança, qualidade e desempenho dos dispositivos médicos.
Sistema de Controle Administrativo de Dispositivos Médicos (MDACS)
O MDACS é um sistema de listagem voluntária atualmente em vigor para regular dispositivos médicos. Ele inclui:
- Listagem de Dispositivos: Registro de dispositivos médicos gerais de Classe II, III e IV e dispositivos de diagnóstico in vitro (IVD) de Classe B, C e D.
- Listagem de Comerciantes: Registro de importadores, distribuidores e fabricantes locais.
- Pessoa Responsável Local (LRP): Uma exigência para que fabricantes fora de Hong Kong nomeiem um representante local para gerenciar as obrigações regulatórias.
Principais Funções e Funções
- Controle Pré-mercado: Avaliação de solicitações de listagem com base em padrões internacionais (como ISO 13485).
- Monitoramento Pós-mercado: Gerenciamento de um sistema para relatar e investigar incidentes adversos envolvendo dispositivos médicos.
- Busca de Informações: Manutenção de um banco de dados público para dispositivos e comerciantes listados para aumentar a transparência.
- Padrões de Aquisição: O Departamento de Saúde está exigindo gradualmente que os dispositivos usados em instalações públicas sejam listados no MDACS (Estágio C efetivo em março de 2026).
Medida da Grande Baía (GBA)
Uma medida especial permite que instituições de saúde designadas na GBA usem dispositivos médicos utilizados em hospitais públicos de Hong Kong com necessidade clínica urgente, facilitando a integração da saúde transfronteiriça.
Artigos e guias
Insights da ElendiLabs mapeados para esta região.
20 de março de 2026
Comparação entre ElendiLabs e Arqon: Plataforma Global Inovadora versus Expertise Tradicional em Representação Local para Serviços Regulatórios de Dispositivos Médicos
ElendiLabs se destaca como uma plataforma digital global mais barata e flexível, com cobertura de mais países, artigos gratuitos com insights de consultores verificados e compartilhamento de casos, além de tempos de resposta mais curtos via pareamento instantâneo de projetos; Arqon oferece consultoria tradicional confiável para dispositivos médicos com retenção de licenças locais, suporte de conformidade na UE, EUA e Ásia (ASEAN), além de serviços de grupo para treinamento e desenvolvimento de negócios. ElendiLabs entrega valor superior, acessibilidade e escalabilidade para o sucesso regulatório mundial.
Ler artigo →
19 de março de 2026
Comparação entre ElendiLabs e Pacific Bridge Medical: Plataforma Global Inovadora versus Expertise Tradicional Focada na Ásia em Serviços Regulatórios para Dispositivos Médicos e Farmacêuticos
ElendiLabs se destaca como uma plataforma digital global mais barata e flexível, com cobertura de mais países, artigos gratuitos com insights de consultores verificados e compartilhamento de casos, além de tempos de resposta mais curtos via pareamento instantâneo de projetos; Pacific Bridge Medical oferece consultoria tradicional confiável em regulamentação e desenvolvimento de negócios com representação de agente local, ensaios clínicos e foco exclusivo na Ásia para dispositivos médicos, IVDs, farmacêuticos e biotecnologia. ElendiLabs entrega valor superior, acessibilidade e escalabilidade para o sucesso regulatório mundial.
Ler artigo →
19 de março de 2026
Comparação entre ElendiLabs e Qualtechs: Plataforma Global Inovadora versus Expertise Tradicional Focada na Ásia em Serviços Regulatórios para Dispositivos Médicos e Farmacêuticos
ElendiLabs se destaca como uma plataforma digital global mais barata e flexível, com cobertura de mais países, artigos gratuitos com insights de consultores verificados e compartilhamento de casos, além de tempos de resposta mais curtos via pareamento instantâneo de projetos; Qualtechs oferece consultoria tradicional one-stop confiável e ensaios clínicos com profunda expertise asiática. ElendiLabs entrega valor superior, acessibilidade e escalabilidade para o sucesso regulatório mundial.
Ler artigo →
18 de março de 2026
Comparação entre ElendiLabs e Asia Actual: Plataforma Global Inovadora versus Expertise Tradicional Focada na Ásia em Serviços Regulatórios para Dispositivos Médicos e IVDs
ElendiLabs se destaca como uma plataforma digital global mais barata e flexível, com cobertura de mais países, artigos gratuitos com insights de consultores verificados e compartilhamento de casos, além de tempos de resposta mais curtos via pareamento instantâneo de projetos; Asia Actual oferece representação regulatória local confiável e acesso ao mercado em 16 países da APAC com especialistas experientes. ElendiLabs entrega valor superior, acessibilidade e escalabilidade para o sucesso regulatório mundial.
Ler artigo →
28 de fevereiro de 2026
Navegando pelo Registro Farmacêutico nos Mercados Asiáticos
Esta visão geral detalha as estruturas regulatórias para registro farmacêutico em Hong Kong, Taiwan e países da ASEAN como Indonésia, Malásia, Filipinas, Singapura, Tailândia e Vietnã, incluindo autoridades principais, processos de aplicação e prazos para entrada no mercado.
Ler artigo →
24 de dezembro de 2025
ISO 13485:2016 na prática: guia do SGQ para dispositivos médicos
A ISO 13485 é a norma global de SGQ para empresas de dispositivos médicos. Este artigo explica o que ela é, o que exige (documentação, liderança, projeto, fornecedores, produção e melhoria) e como iniciar a implementação de forma prática e baseada em risco.
Ler artigo →
15 de dezembro de 2025
Portais Globais de Submissão eCTD: Uma Referência Regional para Profissionais Regulatórios
O Documento Técnico Comum Eletrônico (eCTD) é o padrão global para submissões farmacêuticas, mas cada autoridade regulatória mantém seu próprio portal exclusivo e requisitos de autenticação. Este guia fornece um panorama abrangente dos principais portais nas Américas, Europa, Ásia-Pacífico e Oriente Médio, destacando a importância das especificações regionais do Módulo 1 e dos métodos de autenticação digital.
Ler artigo →
2 de novembro de 2025
O Papel e Requisitos da Licença de Atacadista (WDL) em Hong Kong
Uma visão geral da Licença de Atacadista (WDL) obrigatória para a distribuição farmacêutica em Hong Kong, incluindo a definição abrangente de distribuição, responsabilidades de registo de produtos e requisitos específicos de instalação e armazenamento, tudo apresentado em forma narrativa contínua.
Ler artigo →
27 de outubro de 2025
Requisitos e Função da Licença de Atacadista em Hong Kong
Requisitos legais detalhados para obter e utilizar a Licença de Atacadista (WDL) em Hong Kong, incluindo o seu papel central no registo de medicamentos e requisitos específicos para o manuseio de substâncias controladas (Venenos, Drogas Perigosas).
Ler artigo →
22 de outubro de 2025
Cautela e Requisitos Legais para Importar Medicamentos para Hong Kong
Visão geral dos riscos associados a medicamentos estrangeiros não registados e as distinções legais para importação para uso pessoal versus venda comercial em Hong Kong.
Ler artigo →
21 de outubro de 2025
Portaria de Anúncios Médicos Indesejáveis (UMAO) Cap. 231: Protegendo o Público de Alegações Enganosas
Uma ferramenta regulatória em Hong Kong que controla a publicidade de medicamentos e tratamentos alegadamente capazes de prevenir ou tratar doenças listadas (por exemplo, cancro, tuberculose), para proteger a saúde pública contra alegações exageradas ou falsas.
Ler artigo →
20 de outubro de 2025
Diretrizes CP de Farmácias Comunitárias de HK: A Mudança para Cuidados de Saúde Primários e Garantia de Qualidade
As novas Diretrizes CP marcam uma transformação essencial para as farmácias comunitárias de Hong Kong, expandindo seu papel além da dispensação (ASP COP) para incluir serviços formalizados de cuidados primários, gestão de riscos e avaliação de qualidade obrigatória.
Ler artigo →
15 de setembro de 2025
Regulamentação de Suplementos Herbais Chineses em HK: A Divisão entre Alimento e Medicamento
Uma análise da estrutura regulatória para suplementos de ervas chinesas em Hong Kong, destacando a distinção legal entre esses produtos e as Medicinas Chinesas Proprietárias (pCm) registradas.
Ler artigo →
21 de agosto de 2025
Registro de Medicina Chinesa Proprietária (pCm) em HK: Conformidade e Padrões de Qualidade
Uma visão geral abrangente do processo obrigatório de registro de Medicina Chinesa Proprietária (pCm) em Hong Kong, focando nos três pilares regulatórios centrais: Segurança, Eficácia e Qualidade (S.E.Q.).
Ler artigo →
23 de julho de 2025
Guia Completo para o Registro de Medicamentos Genéricos em Hong Kong
Saiba mais sobre o processo de registro simplificado para medicamentos genéricos em Hong Kong, incluindo requisitos de bioequivalência e os benefícios de medicamentos acessíveis.
Ler artigo →
23 de junho de 2025
Acesso ao Mercado de Dispositivos Médicos em Hong Kong: Uma Perspectiva Regulatória
Hong Kong oferece um mercado dinâmico de dispositivos médicos com um sistema de listagem voluntária único, em transição para uma estrutura obrigatória. Este artigo aborda o ambiente regulatório, a classificação, o papel crítico da Pessoa Responsável Local (LRP) e aspectos-chave para navegar na entrada no mercado, tudo baseado em nossas percepções e experiências para um acesso bem-sucedido ao mercado de dispositivos médicos de Hong Kong.
Ler artigo →
23 de junho de 2025
Registro de Dispositivos Médicos em Hong Kong: Um Caminho para o Mercado
O Sistema de Controle Administrativo de Dispositivos Médicos (MDACS) de Hong Kong oferece um caminho de listagem voluntária único para dispositivos médicos. Este artigo descreve o quadro regulatório, o papel essencial da Pessoa Responsável Local (LRP) e o processo simplificado para registro de produtos e conformidade pós-mercado, fornecendo uma rota clara para o mercado, tudo baseado em nossas percepções e experiências para um registro eficiente de dispositivos médicos em Hong Kong.
Ler artigo →
23 de junho de 2025
Registro de Dispositivos Médicos em Hong Kong: Uma Visão Geral
O Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS) oferece um caminho de listagem voluntária para dispositivos médicos e IVDs. Este artigo descreve o cenário regulatório, a classificação, o papel da Pessoa Responsável Local (LRP) e o processo de registro para entrada no mercado, tudo baseado em nossas percepções e experiências para um registro eficiente de dispositivos médicos em Hong Kong.
Ler artigo →
23 de junho de 2025
Registro e Aprovação de Dispositivos Médicos e IVD em Hong Kong
O Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS) oferece um caminho de listagem voluntária para dispositivos médicos e IVDs, com uma futura estrutura obrigatória no horizonte. Este artigo explora o sistema de classificação, o papel crucial da Pessoa Responsável Local (LRP) e o processo de registro para entrada no mercado, tudo baseado em nossas percepções e experiências para um registro eficiente de dispositivos médicos e IVDs em Hong Kong.
Ler artigo →
23 de junho de 2025
Código de Prática para Distribuidores Listados de Dispositivos Médicos em Hong Kong: Um Guia para COP-05
Para distribuidores de dispositivos médicos listados sob o MDACS de Hong Kong, aderir a um Código de Prática específico é crucial para manter canais de distribuição eficazes e a segurança pública. Este artigo, orientado pelo COP-05, detalha suas responsabilidades em áreas como manutenção de registros, manuseio e vigilância pós-mercado, tudo a partir de nossa experiência e insights.
Ler artigo →
23 de junho de 2025
Código de Práticas para Importadores Listados de Dispositivos Médicos em Hong Kong: Um Guia para COP-04
Para importadores de dispositivos médicos listados sob o MDACS de Hong Kong, aderir a um Código de Prática específico é vital para garantir a integridade da cadeia de suprimentos e a segurança pública. Este artigo, guiado pelo COP-04, detalha suas responsabilidades em áreas como manutenção de registros, manuseio e vigilância pós-mercado, tudo a partir de nossa experiência e insights.
Ler artigo →
23 de junho de 2025
Código de Práticas para Fabricantes Locais de Dispositivos Médicos Listados em Hong Kong: Um Guia para COP-03
Fabricantes locais de dispositivos médicos listados sob o MDACS de Hong Kong seguem um Código de Prática que garante qualidade e segurança. Este artigo, orientado pelo COP-03, descreve suas responsabilidades, com foco em sistemas de gestão da qualidade, controle de produção e vigilância pós-mercado para manter os padrões regulatórios, tudo a partir de nossa experiência e insights.
Ler artigo →
23 de junho de 2025
Código de Prática para Organismos de Avaliação da Conformidade (CABs) em Hong Kong: Um Guia para COP-02
Os Organismos de Avaliação da Conformidade (CABs) desempenham um papel vital na verificação da conformidade de dispositivos médicos no MDACS de Hong Kong. Este artigo, orientado pelo Código de Prática COP-02, descreve o processo de reconhecimento, responsabilidades e requisitos operacionais para os CABs, a fim de garantir avaliações objetivas e rigorosas da segurança e desempenho dos dispositivos médicos, tudo a partir de nossa experiência e insights.
Ler artigo →
23 de junho de 2025
Código de Prática para Pessoas Responsáveis Locais (LRPs) em Hong Kong: Um Guia para COP-01
A Pessoa Responsável Local (LRP) é uma pedra angular do Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS). Este artigo, orientado pelo Código de Prática COP-01, descreve as amplas responsabilidades e deveres dos LRPs em garantir a segurança, qualidade e desempenho dos dispositivos médicos ao longo de seu ciclo de vida, tudo a partir de nossa experiência e conhecimento.
Ler artigo →
23 de junho de 2025
Dispositivos Médicos Personalizados em Hong Kong: Um Guia para TR-009
À medida que a tecnologia médica avança em direção ao cuidado individualizado do paciente, o MDACS de Hong Kong emitiu orientações específicas sobre Dispositivos Médicos Personalizados. Este artigo, guiado pela Referência Técnica TR-009, define e categoriza esses dispositivos—Feitos Sob Medida, Compatíveis com o Paciente e Adaptáveis—e esclarece sua aplicabilidade regulatória, tudo a partir de nossa experiência e insights.
Ler artigo →
23 de junho de 2025
Dispositivos Médicos de Inteligência Artificial (AI-MD) em Hong Kong: Um Guia para TR-008
À medida que a IA transforma a saúde, o MDACS de Hong Kong fornece orientações específicas para Dispositivos Médicos de Inteligência Artificial (AI-MDs). Este artigo, orientado pela Referência Técnica TR-008, aborda as definições, considerações regulatórias únicas e requisitos de documentação essenciais para AI-MDs, incluindo aqueles com Capacidade de Aprendizado Contínuo (CLC), tudo a partir de nossa experiência e insights.
Ler artigo →

23 de junho de 2025
Princípios Essenciais de Segurança e Desempenho para Dispositivos Médicos em Hong Kong: Uma Análise Profunda do TR-004
A base da regulamentação de dispositivos médicos no MDACS de Hong Kong é construída sobre os Princípios Essenciais de Segurança e Desempenho. Este artigo, especificamente orientado pela Referência Técnica TR-004, detalha esses requisitos fundamentais que os fabricantes devem integrar em cada etapa do ciclo de vida de um dispositivo para garantir a segurança do paciente e do usuário, tudo baseado em nossas percepções e experiências para uma regulamentação robusta de dispositivos médicos em Hong Kong.
Ler artigo →
23 de junho de 2025
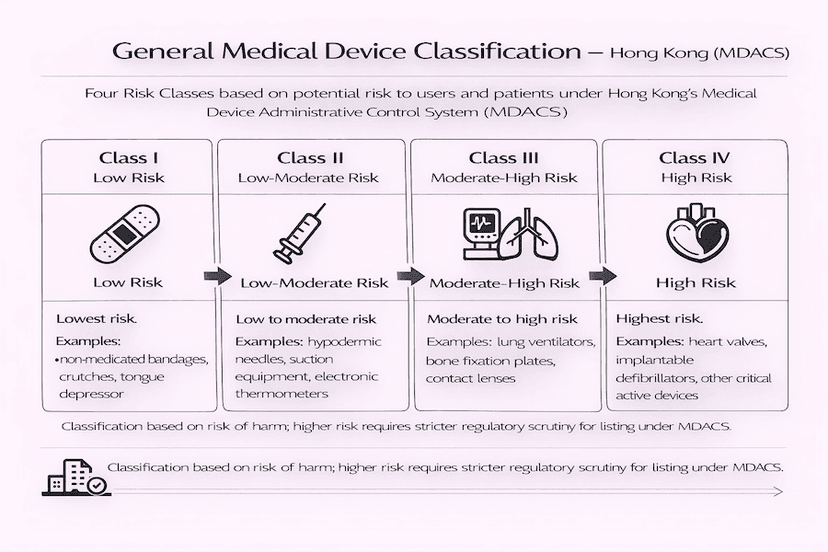
Classificação de Dispositivos Médicos Gerais em Hong Kong: Um Guia para TR-003
Compreender a classificação baseada em risco de dispositivos médicos gerais é fundamental para o acesso ao mercado em Hong Kong. Este artigo, guiado pela Referência Técnica TR-003, detalha as regras e fatores que determinam a classe de risco de um dispositivo sob o Sistema de Controle Administrativo de Dispositivos Médicos (MDACS), tudo baseado em nossas percepções e experiências para uma classificação eficiente de dispositivos médicos em Hong Kong.
Ler artigo →

23 de junho de 2025
Resumo da Documentação Técnica (STED) para Dispositivos Médicos em Hong Kong: Um Guia para TR-002
A Documentação Técnica Resumida (DTR) é um componente crucial das aplicações de listagem de dispositivos médicos sob o MDACS de Hong Kong. Este artigo, guiado pela Referência Técnica TR-002, explica o propósito e o conteúdo necessário da DTR para demonstrar conformidade com os Princípios Essenciais de Segurança e Desempenho, tudo baseado em nossas percepções e experiências para uma documentação de dispositivos médicos simplificada em Hong Kong.
Ler artigo →
23 de junho de 2025
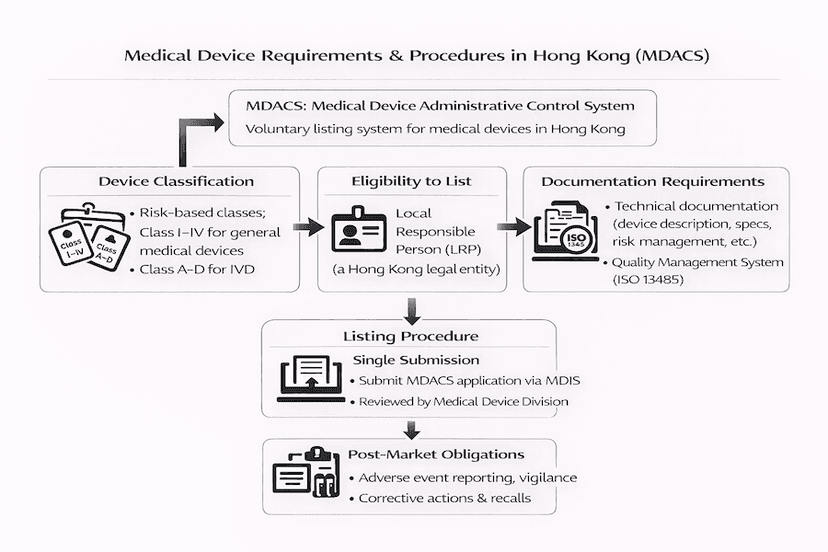
Registro de Dispositivos Médicos em Hong Kong: Requisitos e Procedimentos Essenciais
Um guia abrangente sobre os requisitos e procedimentos essenciais para o registro de dispositivos médicos sob o Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS), tudo baseado em nossas percepções e experiências para um registro eficiente de dispositivos médicos em Hong Kong.
Ler artigo →
16 de junho de 2025
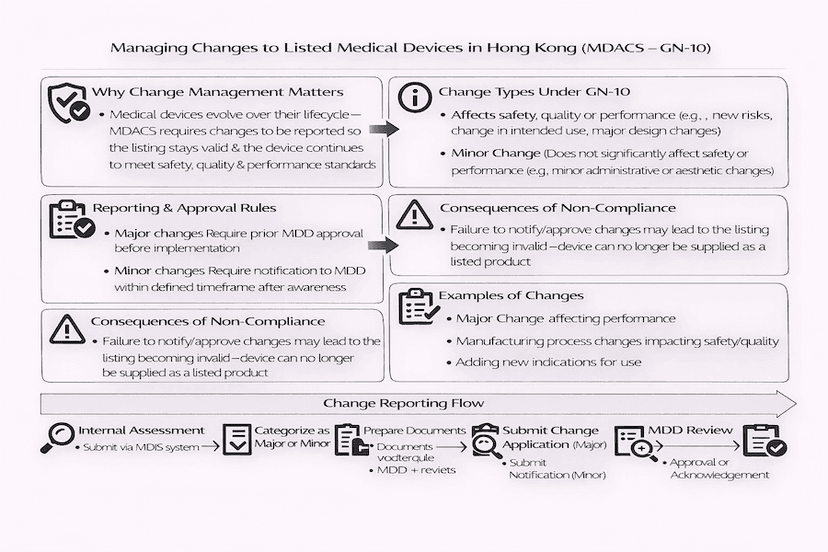
Gerenciando Mudanças para Dispositivos Médicos Listados em Hong Kong: Um Guia para GN-10
Mudanças em dispositivos médicos listados sob o Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS) requerem gerenciamento e relatórios cuidadosos. Este artigo, orientado pelo GN-10, explica como as Pessoas Responsáveis Locais (LRPs) devem categorizar, gerenciar e relatar mudanças maiores e menores para garantir a conformidade contínua e a segurança do paciente, com base em nossas percepções.
Ler artigo →
16 de junho de 2025
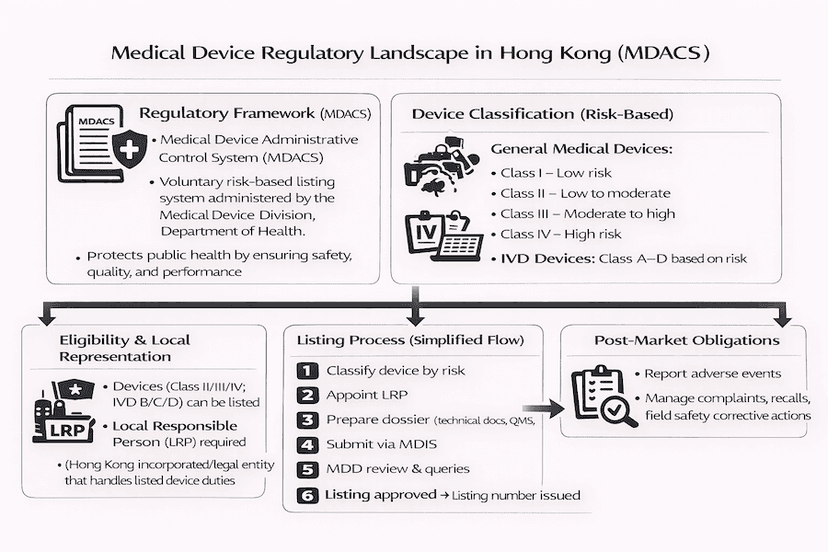
Navegando pelo Cenário Regulatório de Dispositivos Médicos em Hong Kong
Uma visão detalhada do Sistema de Controle Administrativo de Dispositivos Médicos (MDACS) em Hong Kong, cobrindo a classificação de dispositivos, o processo abrangente de listagem, obrigações pós-mercado e o futuro da regulamentação obrigatória, compartilhada a partir de nossas percepções e experiências.
Ler artigo →
15 de junho de 2025
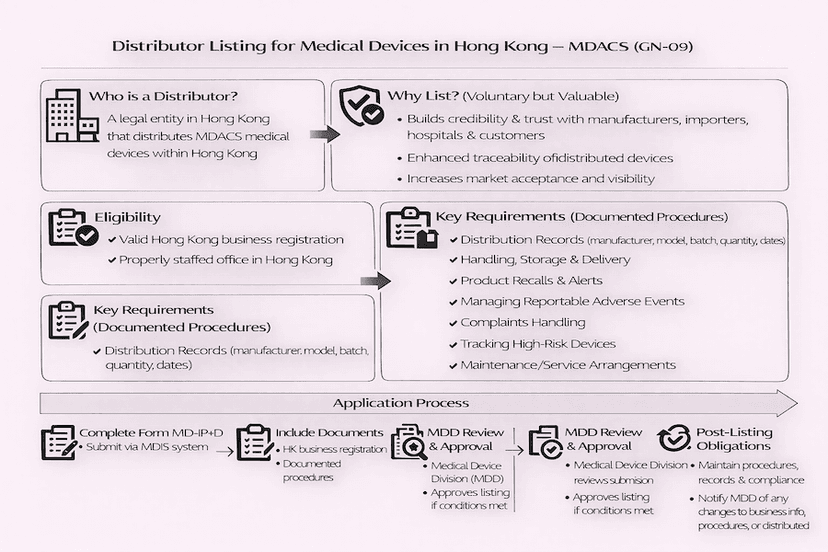
Procedimentos de Listagem para Distribuidores de Dispositivos Médicos em Hong Kong: Um Guia para GN-09
Este artigo descreve o processo de aplicação para distribuidores de dispositivos médicos que buscam ser listados sob o Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS), conforme detalhado no GN-09. Ele abrange elegibilidade, requisitos-chave para procedimentos documentados e o processo de submissão para aprimorar a rastreabilidade e a segurança pública, com base em nossas percepções.
Ler artigo →
14 de junho de 2025
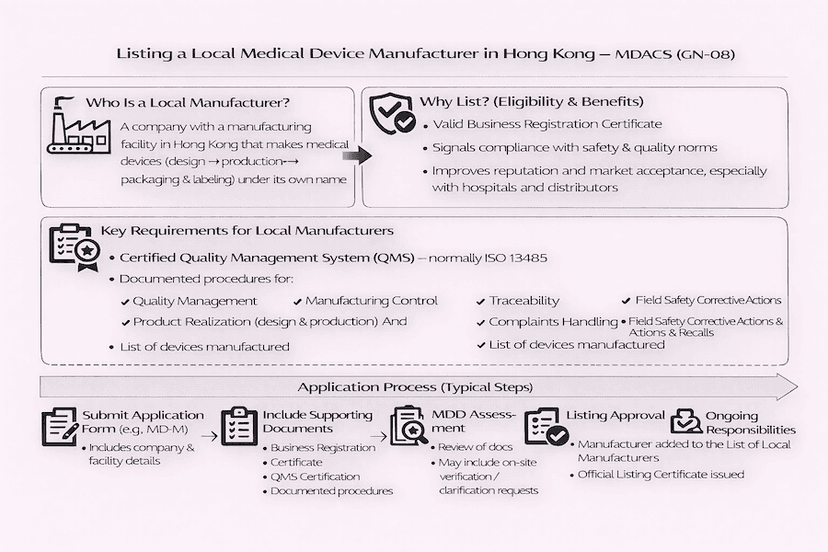
Procedimentos de Listagem para Fabricantes Locais de Dispositivos Médicos em Hong Kong: Um Guia para GN-08
Este artigo detalha o processo de aplicação para fabricantes locais de dispositivos médicos que buscam ser listados sob o Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS), conforme orientado pelo GN-08. Ele abrange elegibilidade, requisitos do sistema de gestão da qualidade e o processo de submissão, tudo baseado em nossas percepções e experiências para uma fabricação eficaz de dispositivos médicos em Hong Kong.
Ler artigo →
14 de junho de 2025
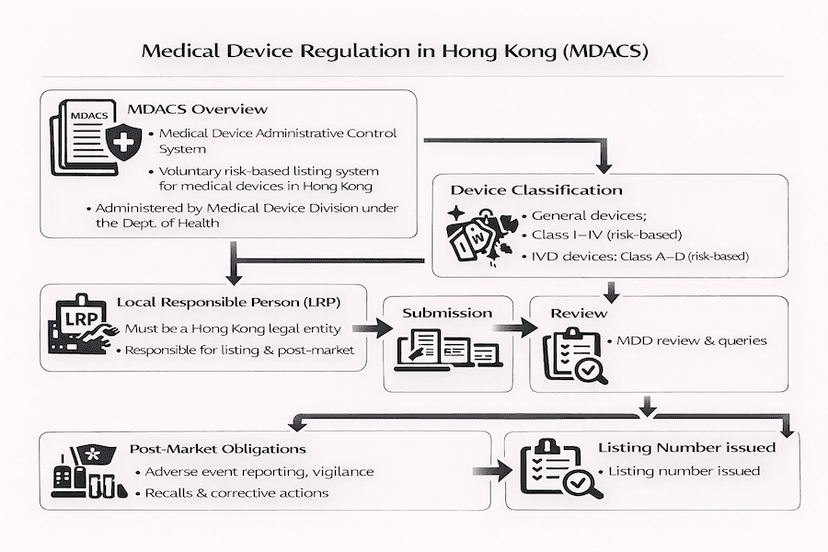
Navegando nas Regulamentações de Dispositivos Médicos em Hong Kong: A Estrutura MDACS
O Sistema de Controle Administrativo de Dispositivos Médicos (MDACS) de Hong Kong fornece uma estrutura robusta, embora atualmente voluntária, para a regulamentação de dispositivos médicos. Este artigo explora as principais características do sistema, incluindo a classificação de dispositivos, o processo de listagem, o papel crucial das Pessoas Responsáveis Locais (LRPs) e sua importância crescente para o acesso ao mercado e a aquisição pública, tudo a partir de nossas percepções e experiências.
Ler artigo →
2 de junho de 2025
Procedimentos de Listagem para Dispositivos Médicos de Diagnóstico In Vitro de Classe B, C e D em Hong Kong: Um Guia para GN-06
Este artigo detalha o processo de aplicação para listar Dispositivos Médicos de Diagnóstico In Vitro de Classe B, C e D (IVDMDs) sob o Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS), conforme orientado pelo GN-06. Ele abrange classificação, elegibilidade, requisitos de submissão e a aplicação online via MDIS, tudo baseado em nossos insights e experiência para uma listagem eficiente de IVDMD em Hong Kong.
Ler artigo →
1 de junho de 2025
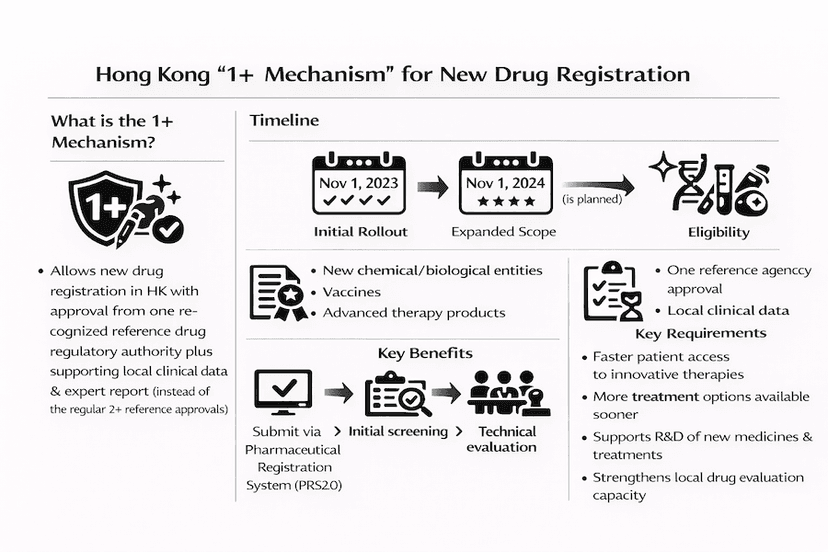
O Mecanismo "1+": Acelerando o Registro de Novos Medicamentos em Hong Kong
Saiba mais sobre o inovador mecanismo "1+" de registro de medicamentos de Hong Kong, seu impacto no acesso dos pacientes a novos tratamentos e seu papel na promoção do desenvolvimento da saúde na Grande Baía, tudo através de nossas percepções e experiências.
Ler artigo →

24 de maio de 2025
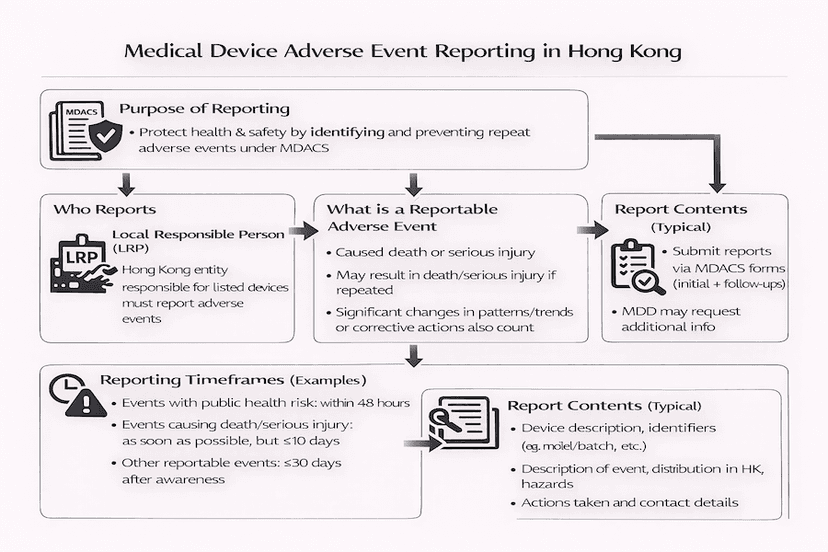
Relato de Eventos Adversos de Dispositivos Médicos em Hong Kong: Um Guia para LRPs
A notificação de eventos adversos é um componente crítico do Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS), com o objetivo de melhorar a saúde e a segurança pública. Este artigo descreve os requisitos e responsabilidades das Pessoas Responsáveis Locais (LRPs) na notificação de eventos adversos relacionados a dispositivos médicos listados, com base em nossas percepções.
Ler artigo →
17 de maio de 2025
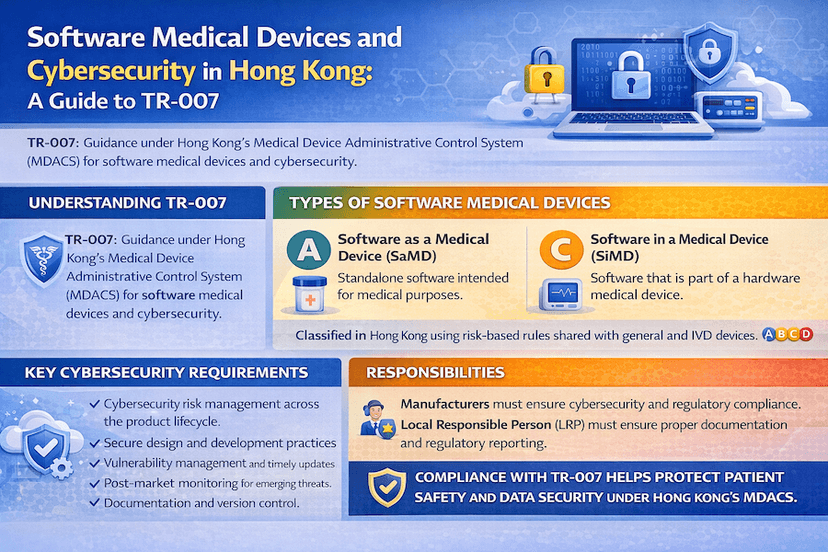
Dispositivos Médicos de Software e Cibersegurança em Hong Kong: Um Guia para o TR-007
À medida que o software desempenha um papel cada vez mais vital na saúde, o MDACS de Hong Kong aborda sua regulamentação, incluindo a cibersegurança. Este artigo, guiado pela Referência Técnica TR-007, descreve a definição de Software como Dispositivo Médico (SaMD) e Software em um Dispositivo Médico (SiMD), além das considerações cruciais de cibersegurança para fabricantes e LRPs, tudo baseado em nossas percepções e experiências para uma cibersegurança robusta de dispositivos médicos em Hong Kong.
Ler artigo →
10 de maio de 2025
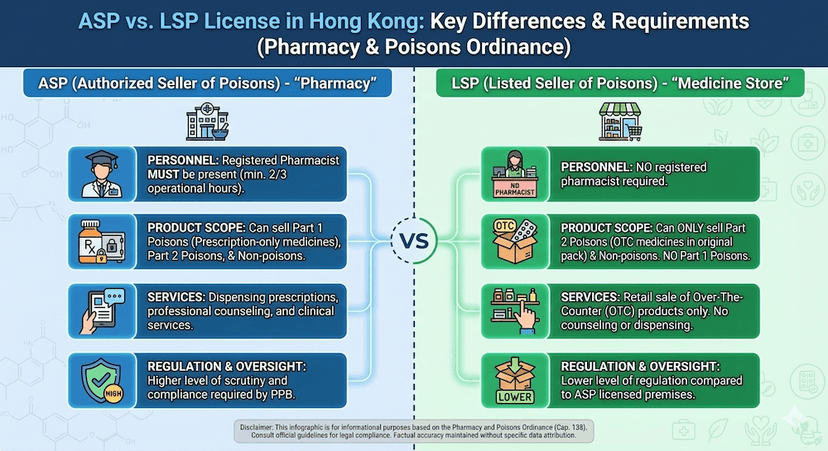
Licença ASP vs LSP: Qual Você Precisa?
Aprenda as diferenças entre a Licença de Vendedor Autorizado de Venenos (ASP) e a Licença de Vendedor Listado de Venenos (LSP) e determine qual é a certa para o seu negócio.
Ler artigo →
3 de maio de 2025
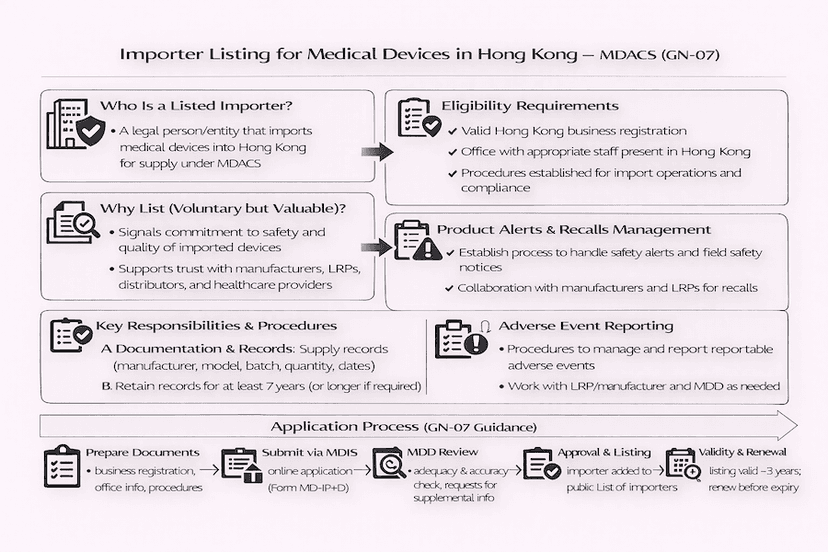
Procedimentos de Listagem para Importadores de Dispositivos Médicos em Hong Kong: Um Guia para GN-07
Para entidades que importam dispositivos médicos para Hong Kong, o Sistema de Controle Administrativo de Dispositivos Médicos (MDACS) oferece um esquema de listagem voluntária para importadores, orientado pela GN-07. Este artigo detalha a elegibilidade, os passos de aplicação e os principais requisitos para a listagem como importador de dispositivos médicos, com base em nossas percepções e experiências para uma importação eficiente de dispositivos médicos em Hong Kong.
Ler artigo →
18 de abril de 2025
Registro de Dispositivos Médicos em Hong Kong: Uma Visão Geral do Mercado e da Regulamentação
Hong Kong apresenta um mercado crescente e dinâmico para dispositivos médicos, governado pelo Sistema de Controle Administrativo de Dispositivos Médicos (MDACS). Este artigo descreve o cenário regulatório, as principais tendências de mercado, a classificação de dispositivos e o processo geral de registro e acesso ao mercado nesta região em evolução, tudo baseado em nossas percepções e experiências.
Ler artigo →
17 de abril de 2025
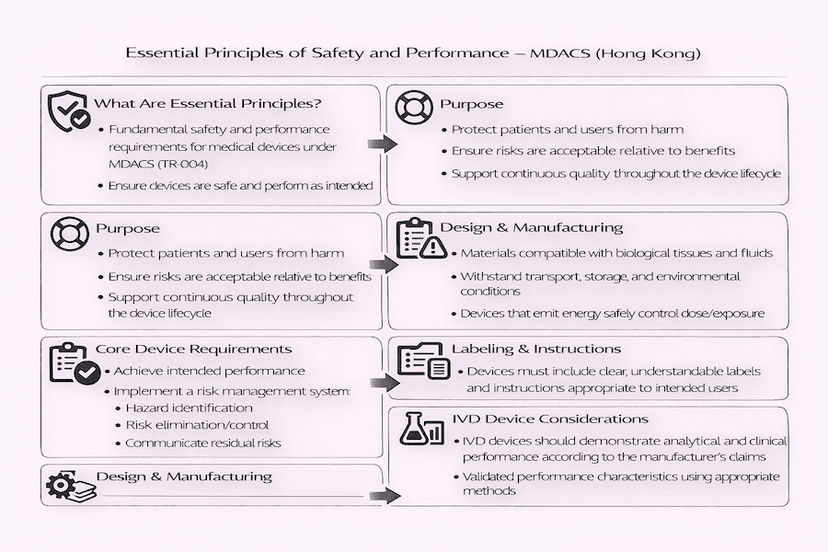
Princípios Essenciais de Segurança e Desempenho para Dispositivos Médicos em Hong Kong: Compreendendo TR-001 e TR-004
A segurança e o desempenho dos dispositivos médicos em Hong Kong são fundamentados por um conjunto de 'Princípios Essenciais', detalhados nas Referências Técnicas TR-001 e TR-004 do MDACS. Este artigo explora esses requisitos fundamentais que os fabricantes devem atender nas fases de design, fabricação e pós-mercado dos dispositivos médicos, a partir de nossas percepções e experiências para uma regulamentação robusta de dispositivos médicos em Hong Kong.
Ler artigo →
12 de abril de 2025
Registro de Produto de Dispositivo Médico em Hong Kong: Uma Abordagem Focada
Navegar pela conformidade regulatória de dispositivos médicos em Hong Kong é crucial para o acesso ao mercado. Este artigo destaca serviços focados em preparar produtos para o Sistema de Controle Administrativo de Dispositivos Médicos (MDACS) e agilizar o processo de registro para uma entrada eficiente no mercado, com base em nossas percepções.
Ler artigo →
6 de abril de 2025
Registro Global de Dispositivos Médicos: Expectativas Regulatórias em Mercados Chave
Levar um único dispositivo médico a vários mercados exige a compreensão de expectativas regulatórias variadas, que estão longe de ser um exercício de "copiar e colar". As principais diferenças incluem o foco da UE na evidência clínica (MDR), a dependência dos EUA na equivalência substancial (510(k)) e a revisão altamente orientada a processos do Japão, enfatizando a necessidade de uma estratégia global robusta e o potencial aproveitamento de programas como o **MDSAP**.
Ler artigo →
21 de março de 2025
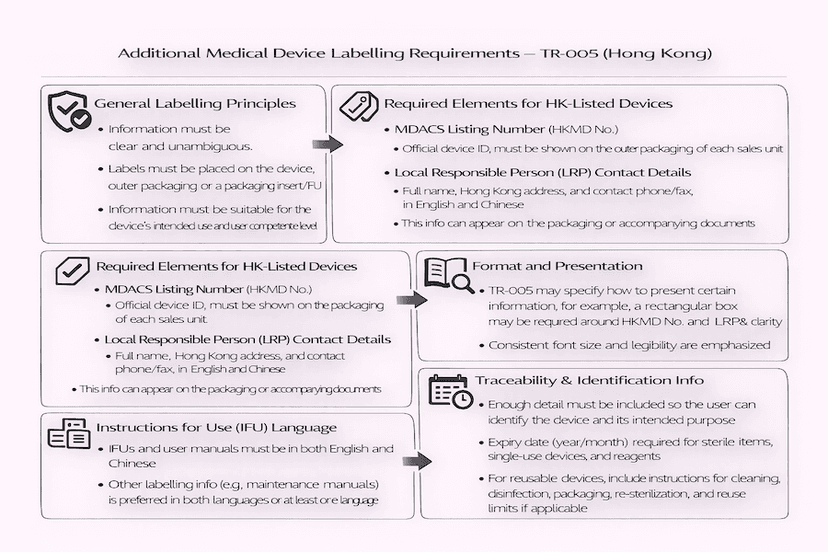
Requisitos Adicionais de Rotulagem de Dispositivos Médicos em Hong Kong: Compreendendo o TR-005
Além dos Princípios Essenciais gerais, o Sistema de Controle Administrativo de Dispositivos Médicos de Hong Kong (MDACS) impõe requisitos adicionais específicos de rotulagem para dispositivos médicos. Este artigo, orientado pela Referência Técnica TR-005, detalha esses elementos cruciais para garantir uma comunicação clara e conformidade no mercado local, tudo baseado em nossas percepções e experiências para uma rotulagem eficaz de dispositivos médicos em Hong Kong.
Ler artigo →
17 de março de 2025
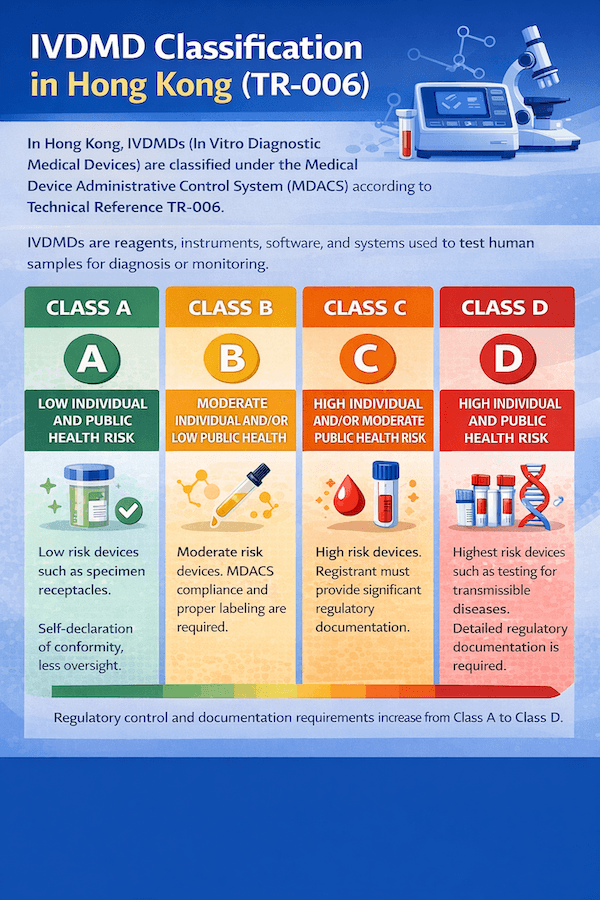
Classificação de Dispositivos Médicos de Diagnóstico In Vitro (IVDMDs) em Hong Kong: Um Guia para TR-006
A classificação de Dispositivos Médicos de Diagnóstico In Vitro (IVDMDs) em Hong Kong é um sistema baseado em risco, crucial para a conformidade regulatória. Este artigo, orientado pela Referência Técnica TR-006, descreve os princípios e categorias que determinam a classe de risco de um IVDMD sob o Sistema de Controle Administrativo de Dispositivos Médicos (MDACS), tudo baseado em nossas percepções e experiências para uma classificação eficiente de IVDMD em Hong Kong.
Ler artigo →
5 de março de 2025
Transformação Digital na Gestão de Farmácias
Como soluções de software modernas estão revolucionando as operações farmacêuticas, melhorando a eficiência e aprimorando o atendimento ao paciente na era digital.
Ler artigo →

28 de janeiro de 2025
Melhores Práticas de Farmacovigilância em Hong Kong
Diretrizes essenciais para a notificação de eventos adversos e conformidade com a farmacovigilância na indústria farmacêutica de Hong Kong.
Ler artigo →
16 de janeiro de 2025
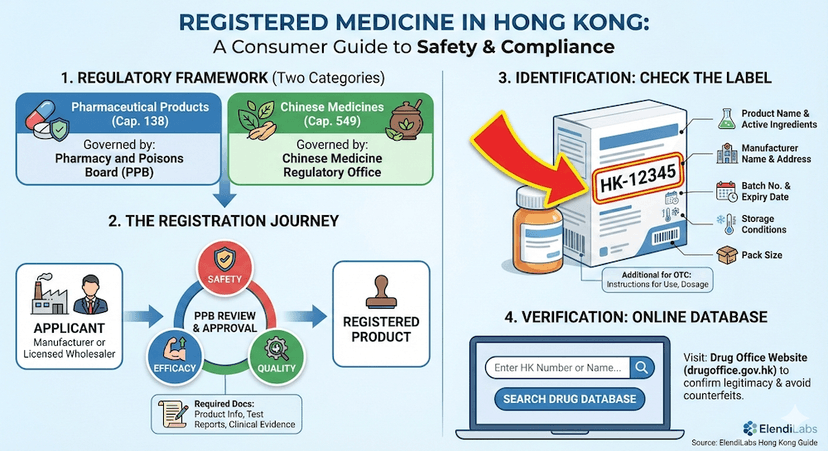
Entendendo a Medicina Registrada em Hong Kong: Um Guia Completo
Saiba mais sobre o sistema de registro de medicamentos de Hong Kong, os requisitos legais e como identificar medicamentos registrados para garantir segurança e eficácia.
Ler artigo →
15 de janeiro de 2025
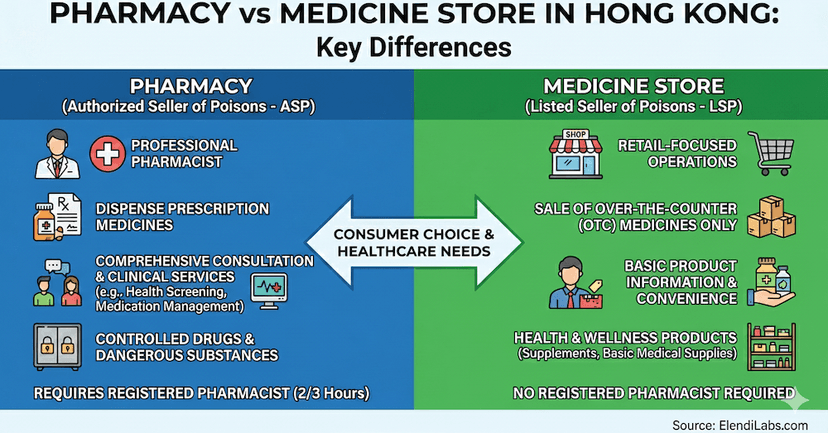
Farmácia vs Loja de Medicamentos: Compreendendo as Principais Diferenças
Uma farmácia possui um farmacêutico licenciado para dispensar medicamentos sob prescrição, enquanto uma drogaria foca em itens de venda livre. Descubra as principais diferenças legais e de serviço aqui.
Ler artigo →

20 de dezembro de 2024
Regulamentações de Importação e Exportação para Produtos Farmacêuticos
Navegue pelo complexo cenário das regulamentações de importação e exportação de produtos farmacêuticos em Hong Kong com este guia detalhado.
Ler artigo →
15 de outubro de 2024
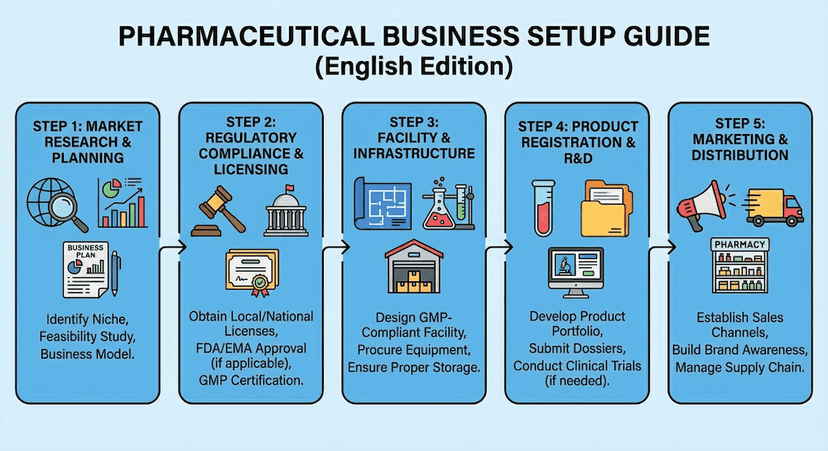
Configurando Seu Negócio Farmacêutico em Hong Kong
Guia passo a passo para estabelecer um negócio farmacêutico em Hong Kong, desde licenciamento até requisitos operacionais.
Ler artigo →
10 de agosto de 2024
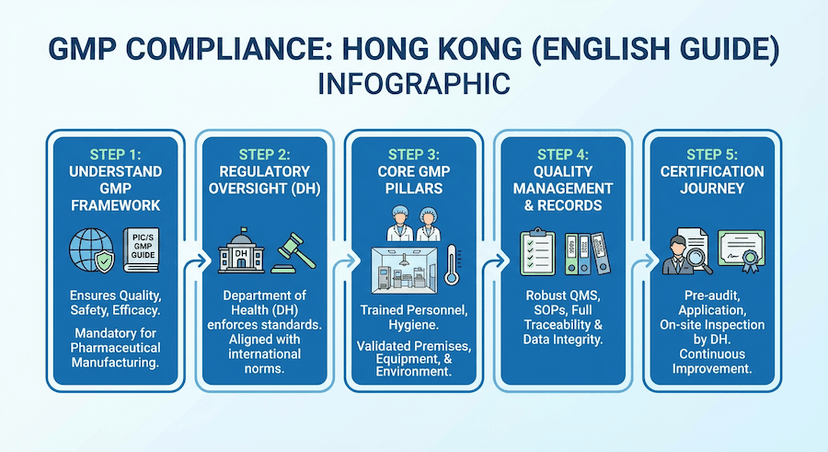
Conformidade com as Boas Práticas de Fabricação (BPF) em Hong Kong
Requisitos essenciais e melhores práticas para implementar a conformidade com GMP em instalações de fabricação farmacêutica.
Ler artigo →
20 de julho de 2024
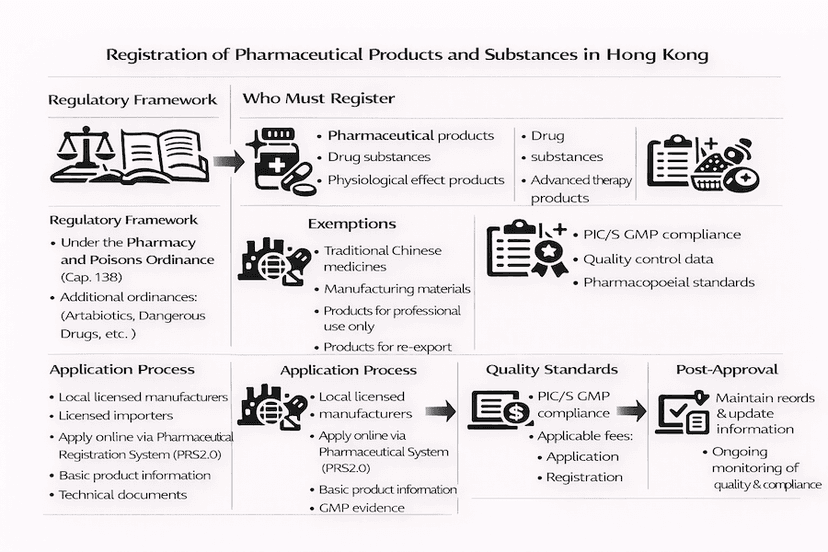
Guia Profissional: Registro de Produtos e Substâncias Farmacêuticas em Hong Kong
Um guia abrangente para profissionais de saúde e partes interessadas da indústria sobre os requisitos de registro, procedimentos e conformidade para produtos e substâncias farmacêuticas em Hong Kong.
Ler artigo →
5 de junho de 2024
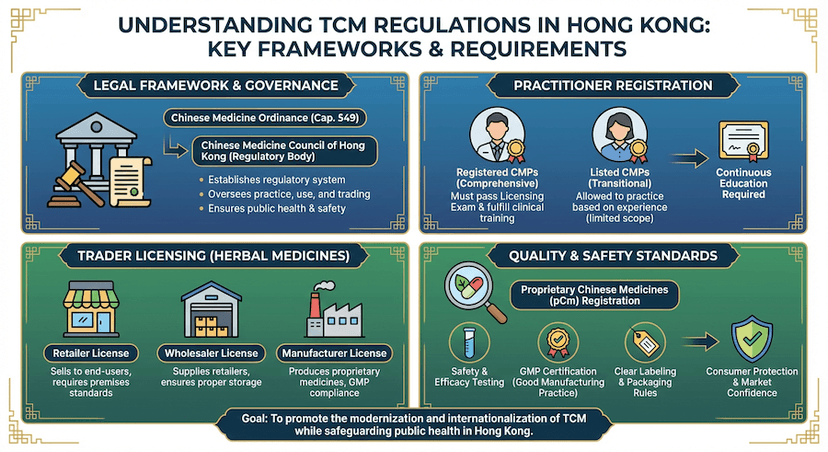
Regulamentações de Medicina Tradicional Chinesa (MTC) em Hong Kong
Guia abrangente sobre as regulamentações da Medicina Tradicional Chinesa, incluindo registro de praticantes e licenciamento de medicina chinesa.
Ler artigo →
10 de maio de 2024
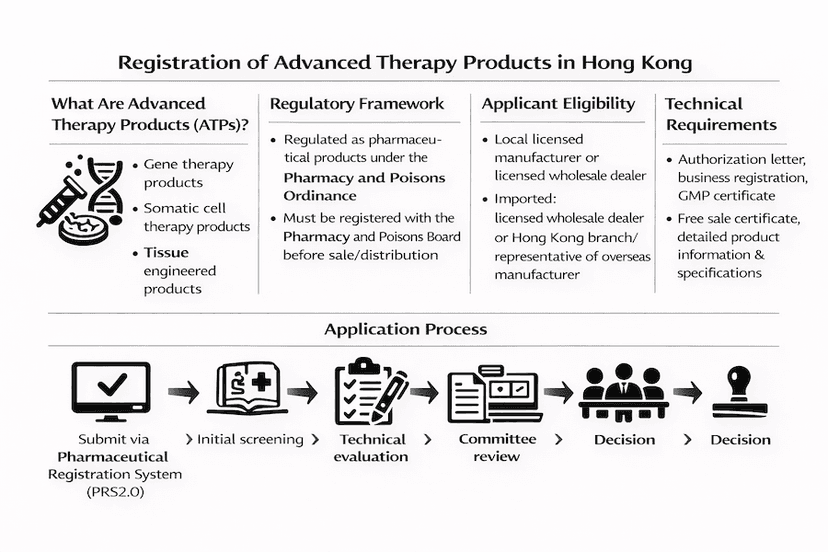
Registro de Produtos de Terapia Avançada em Hong Kong: Um Guia Abrangente
Saiba mais sobre o processo de registro para produtos de terapia avançada (ATPs) em Hong Kong, incluindo terapia gênica, terapia com células somáticas e produtos de engenharia de tecidos.
Ler artigo →
20 de março de 2024
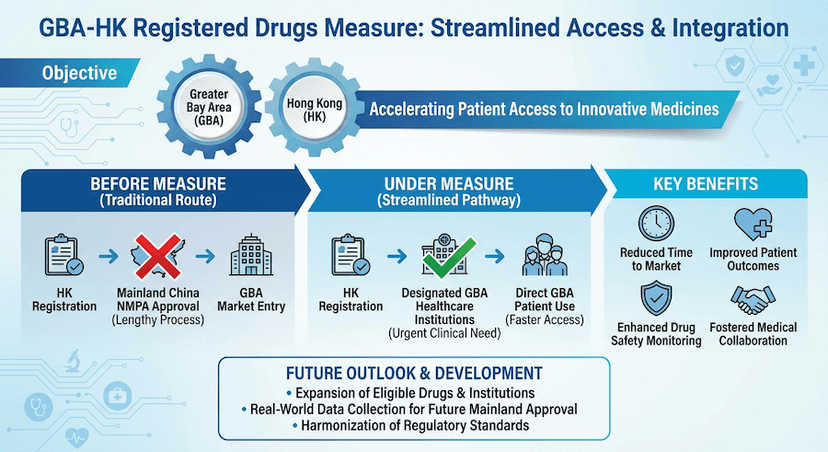
Usando Medicamentos e Dispositivos Médicos Registrados em Hong Kong na Grande Área da Baía: Um Guia Abrangente
Saiba mais sobre a medida inovadora que permite que instituições de saúde designadas na Grande Área da Baía utilizem medicamentos e dispositivos médicos registrados em Hong Kong, facilitando o acesso a cuidados de saúde para os residentes de Hong Kong.
Ler artigo →
20 de março de 2024
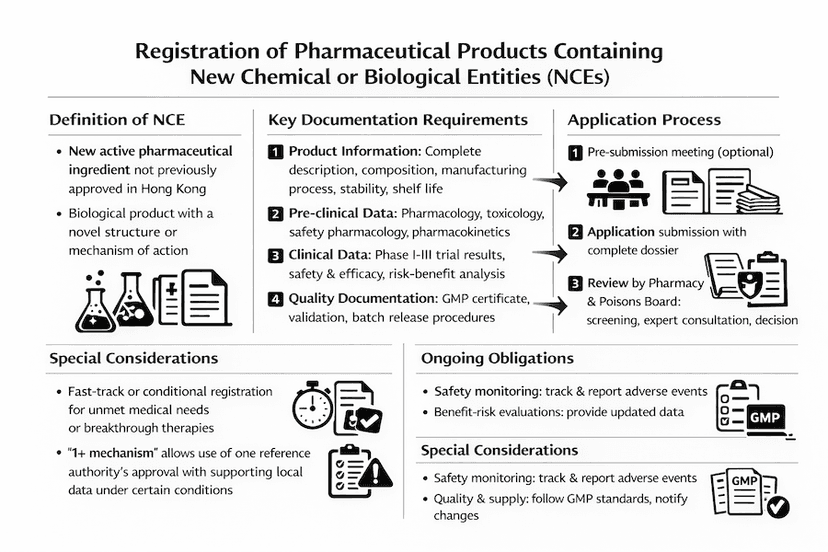
Registro de Produtos Farmacêuticos Contendo uma Nova Entidade Química ou Biológica em Hong Kong
Um guia abrangente sobre o processo de registro de produtos farmacêuticos contendo novas entidades químicas ou biológicas em Hong Kong, incluindo requisitos, procedimentos e considerações regulatórias.
Ler artigo →
20 de fevereiro de 2024
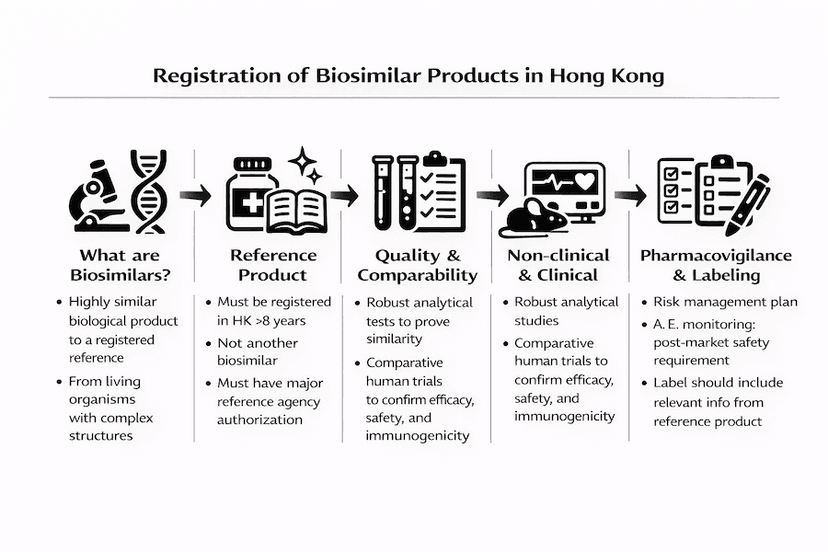
Registro de Produtos Biossimilares em Hong Kong: Um Guia Abrangente
Saiba mais sobre o processo de registro de produtos biossimilares em Hong Kong, incluindo requisitos, documentação e considerações especiais para esses medicamentos biológicos complexos.
Ler artigo →