Quer estudos de caso reais? 10 segundos para se cadastrar
Junte-se à plataforma
Precisa de Ajuda Regulatória? Experimente Nossa Plataforma
Publique suas perguntas regulatórias ou solicite orçamentos de consultores farmacêuticos verificados em todo o mundo. Conecte-se com especialistas do seu mercado.
20 de julho de 2024
Aproximadamente 5 minutos
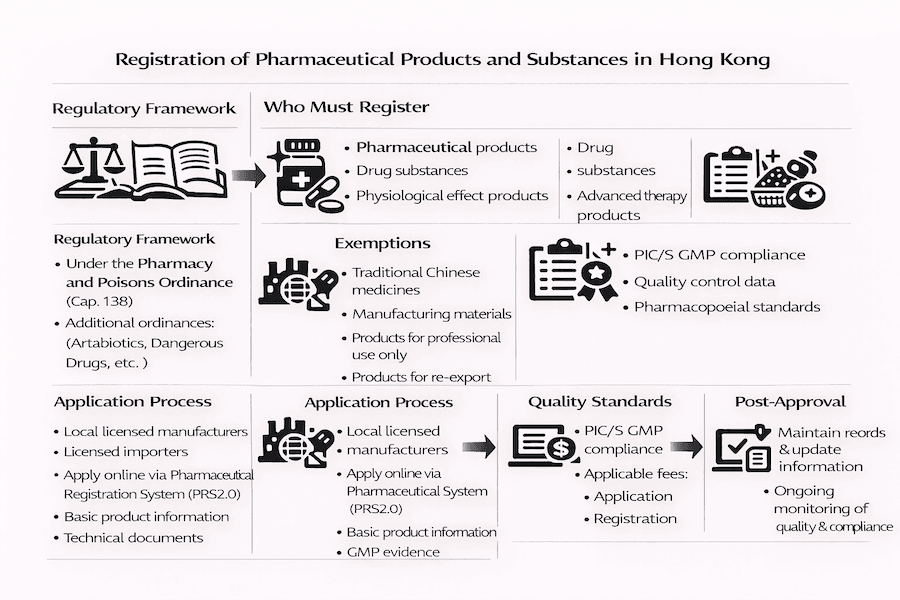
Guia Profissional: Registro de Produtos e Substâncias Farmacêuticas em Hong Kong
Este guia fornece informações essenciais para profissionais de saúde, fabricantes e distribuidores sobre o registro de produtos e substâncias farmacêuticas em Hong Kong.
Estrutura Regulatória
Legislação Reguladora
-
Ordinança de Farmácia e Venenos (Cap. 138)
- Legislação primária para produtos farmacêuticos
- Requisitos e procedimentos de registro
- Disposições de aplicação
-
Ordinanças de Apoio
- Ordinança de Antibióticos (Cap. 137)
- Ordinança de Drogas Perigosas (Cap. 134)
- Ordinança de Publicidade Médica Indesejável (Cap. 231)
Requisitos de Registro
Produtos que Requerem Registro
-
Produtos Farmacêuticos
- Produtos com alegações medicinais
- Produtos contendo substâncias medicamentosas
- Produtos que afetam funções fisiológicas
- Produtos de terapia avançada
-
Isenções
- Medicamentos tradicionais chineses
- Materiais de fabricação
- Produtos de uso profissional
- Produtos de reexportação
- Produtos de ensaio clínico
Processo de Aplicação
Critérios de Elegibilidade
-
Fabricantes Locais
- Deve ser um fabricante licenciado
- Deve ter certificação GMP
- Deve cumprir os padrões PIC/S
-
Importadores
- Deve ser um comerciante atacadista licenciado
- Deve ter autorização do fabricante
- Deve atender aos requisitos de importação
Documentação Necessária
-
Informações Básicas
- Certificado de registro empresarial
- Autorização do fabricante
- Autorização de aplicação
-
Documentação Técnica
- Certificado GMP
- Certificado de Livre Venda
- Especificações do produto
- Dados de controle de qualidade
-
Requisitos Especiais
- Documentação de materiais de origem animal
- Declarações de múltiplos fabricantes
- Dados de bioequivalência (se aplicável)
Padrões de Qualidade
Requisitos de Fabricação
-
Conformidade com GMP
- Padrões GMP do PIC/S
- Sistema de gestão da qualidade
- Requisitos de instalação
-
Controle de Qualidade
- Especificações de liberação
- Dados de estabilidade
- Protocolos de validação
Padrões Farmacopeiais
- Farmacopeia Chinesa
- Farmacopeia Britânica
- Farmacopeia Europeia
- Farmacopeia Internacional
- Farmacopeia Japonesa
- Farmacopeia dos Estados Unidos
Submissão de Aplicação
Sistema Online
- Use o sistema PRS 2.0
- Envie documentos eletrônicos
- Pague a taxa de aplicação (HK$1.100)
Documentos de Apoio
- Envie certificados originais
- Forneça cópias autenticadas
- Inclua traduções se necessário
Requisitos Pós-Aprovação
Taxa de Registro
- HK$1.370 por produto
- Pagável após aprovação
- Necessária para coleta de certificado
Obrigações de Conformidade
-
Documentação
- Manter registros
- Atualizar informações
- Relatar mudanças
-
Garantia de Qualidade
- Testes regulares
- Monitoramento de estabilidade
- Tratamento de reclamações
Considerações Especiais
Direitos de Patente
- O conselho não considera patentes
- Candidatos responsáveis pela conformidade
- Riscos potenciais de infração
- Consulta legal recomendada
Múltiplos Fabricantes
- Caminho de fabricação único preferido
- Caminhos alternativos requerem aplicações separadas
- Documentação clara dos papéis necessária
Acompanhamento da Aplicação
Monitoramento de Progresso
- Acompanhe o status da aplicação
- Cite a referência do arquivo
- Contate a Unidade de Registro de Medicamentos
- Acompanhe conforme necessário
Notas Importantes
Conformidade Legal
- Siga a legislação atual
- Monitore atualizações regulatórias
- Mantenha documentação
- Assegure padrões de qualidade
Responsabilidade Profissional
- Verifique a elegibilidade do produto
- Assegure documentação completa
- Monitore o progresso da aplicação
- Mantenha a conformidade
Informações de Contato
Escritório de Medicamentos, Departamento de Saúde
- Website: www.drugoffice.gov.hk
Recursos Adicionais
- Legislação: www.elegislation.gov.hk
Preços Imbatíveis
Taxas transparentes e competitivas para registro de dispositivos médicos em Hong Kong.
Farmacêutico registrado · Engenheiro de IA · Diretor, ElendiLabs
Farmacêutico registrado, engenheiro de IA, fundador da HKHAIS e especialista em SEO/GEO para o domínio farmacêutico e de dispositivos médicos.
Pergunte Qualquer Coisa
Entraremos em contato pessoalmente.
100% de taxa de resposta • Resposta em até 7 dias úteis
Precisa de Orientação Especializada?
Entre em contato conosco em contact@elendilabs.com / +852 4416 5550