Quer estudos de caso reais? 10 segundos para se cadastrar
Junte-se à plataforma
Precisa de Ajuda Regulatória? Experimente Nossa Plataforma
Publique suas perguntas regulatórias ou solicite orçamentos de consultores farmacêuticos verificados em todo o mundo. Conecte-se com especialistas do seu mercado.
10 de agosto de 2024
Aproximadamente 5 minutos
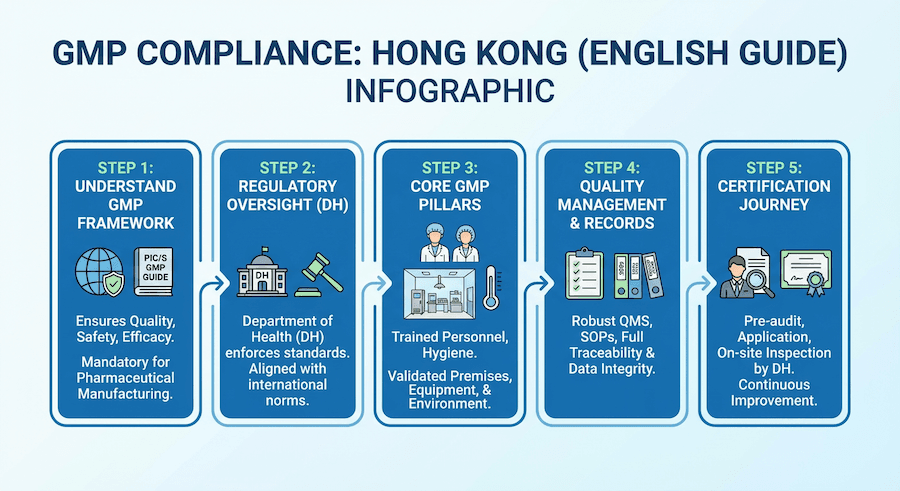
Conformidade com as Boas Práticas de Fabricação (BPF) em Hong Kong
As Boas Práticas de Fabricação (BPF) são um sistema crítico de garantia de qualidade que assegura que os produtos farmacêuticos sejam produzidos e controlados de forma consistente de acordo com os padrões de qualidade. Em Hong Kong, a conformidade com as BPF é obrigatória para todos os fabricantes farmacêuticos.
Compreendendo os Requisitos das BPF
As BPF abrangem todos os aspectos da produção, desde matérias-primas, instalações e equipamentos até treinamento e higiene pessoal dos funcionários. O objetivo principal é prevenir contaminações, trocas e erros durante a fabricação.
Princípios Chave das BPF:
- Sistemas de gestão da qualidade
- Qualificações e treinamento do pessoal
- Padrões de instalações e equipamentos
- Documentação e manutenção de registros
- Controles de produção
- Testes de controle de qualidade
- Armazenamento e distribuição
Estrutura das BPF em Hong Kong
O Escritório de Medicamentos do Departamento de Saúde supervisiona a conformidade com as BPF sob a Lei de Farmácia e Venenos. Todas as instalações de fabricação devem obter uma Licença de Fabricante e passar por inspeções regulares.
Requisitos Regulatórios:
- Solicitação de Licença de Fabricante
- Projeto e qualificação da instalação
- Validação de equipamentos
- Validação de processos
- Implementação do sistema de qualidade
- Inspeções regulares de conformidade
Projeto e Infraestrutura da Instalação
Requisitos de Construção:
- Localização e construção apropriadas
- Espaço adequado para operações
- Ventilação e manuseio de ar adequados
- Sistemas de água e utilidades
- Instalações de gerenciamento de resíduos
- Segurança e controles de acesso
Áreas de Produção:
- Zonas de fabricação segregadas
- Ambientes controlados
- Design do fluxo de materiais
- Prevenção de contaminação cruzada
- Protocolos de limpeza e desinfecção
Pessoal e Treinamento
Requisitos de Pessoal:
- Designação de Pessoa Qualificada (PQ)
- Gestão de produção
- Pessoal de garantia da qualidade
- Pessoal técnico e de suporte
Programas de Treinamento:
- Treinamento de conscientização sobre BPF
- Treinamento específico para o trabalho
- Protocolos de higiene e segurança
- Requisitos de educação continuada
- Documentação de treinamento
Sistemas de Documentação
Documentação Necessária:
- Manual de qualidade
- Procedimentos Operacionais Padrão (POP)
- Registros de produção de lote
- Registros de controle de qualidade
- Procedimentos de controle de mudanças
- Sistemas de desvio e CAPA
Controle de Documentos:
- Sistemas de controle de versão
- Processos de revisão e aprovação
- Controles de distribuição e acesso
- Procedimentos de retenção e arquivamento
Controle de Qualidade e Testes
Requisitos de Laboratório:
- Instalações de teste qualificadas
- Métodos analíticos validados
- Padrões de referência
- Programas de testes de estabilidade
- Monitoramento ambiental
Protocolos de Teste:
- Testes de matérias-primas
- Controles em processo
- Testes de produtos acabados
- Testes microbiológicos
- Validação de limpeza
Validação e Qualificação
Qualificação de Equipamentos:
- Qualificação de Projeto (QP)
- Qualificação de Instalação (QI)
- Qualificação Operacional (QO)
- Qualificação de Desempenho (QD)
Validação de Processos:
- Validação do design do processo
- Qualificação do processo
- Verificação contínua do processo
- Validação de limpeza
- Validação de sistemas computacionais
Gestão da Cadeia de Suprimentos
Qualificação de Fornecedores:
- Auditorias de fornecedores
- Acordos de qualidade
- Especificações de materiais
- Requisitos de certificado de análise
- Segurança da cadeia de suprimentos
Gestão de Materiais:
- Recebimento e inspeção
- Condições de armazenamento
- Controle de inventário
- Procedimentos de quarentena
- Protocolos de liberação
Deficiências Comuns nas BPF
Questões de Documentação:
- Registros de lote incompletos
- Rastreabilidade inadequada
- Controle de mudanças inadequado
- Controle de documentos deficiente
Instalação e Equipamentos:
- Validação de limpeza inadequada
- Programas de manutenção deficientes
- Controles ambientais insuficientes
- Riscos de contaminação cruzada
Pessoal e Treinamento:
- Registros de treinamento inadequados
- Supervisão insuficiente
- Práticas de higiene deficientes
- Falta de pessoal qualificado
Preparação para Inspeção
Atividades Pré-Inspeção:
- Auditorias de autoavaliação
- Revisão de documentação
- Preparação da equipe
- Prontidão da instalação
- Inspeções simuladas
Durante a Inspeção:
- Cooperação com os inspetores
- Disponibilidade de documentos
- Entrevistas com funcionários
- Visitas às instalações
- Resolução de problemas
Tecnologia e Automação
Sistemas Modernos de BPF:
- Registros de lote eletrônicos
- Sistemas de execução de fabricação
- Sistemas de informação de laboratório
- Sistemas de monitoramento ambiental
- Sistemas de gerenciamento de documentos
Benefícios da Automação:
- Redução de erros humanos
- Melhoria da integridade dos dados
- Aumento da rastreabilidade
- Monitoramento em tempo real
- Eficiência na conformidade
Harmonização Internacional
Diretrizes ICH:
- Q7 Boas Práticas de Fabricação
- Q8 Desenvolvimento Farmacêutico
- Q9 Gestão de Risco de Qualidade
- Q10 Sistema de Qualidade Farmacêutica
- Q11 Desenvolvimento e Fabricação
Reconhecimento Mútuo:
- Membro do PIC/S
- Inspeções internacionais
- Padrões harmonizados
- Cadeias de suprimentos globais
Considerações de Custo
Custos de Implementação:
- Atualizações de instalações
- Investimentos em equipamentos
- Implementações de sistemas
- Programas de treinamento
- Serviços de consultoria
Custos Contínuos:
- Manutenção e calibração
- Testes de qualidade
- Gestão de documentação
- Prontidão para inspeção
- Melhoria contínua
Tendências Futuras
Tecnologias Emergentes:
- Fabricação contínua
- Tecnologia analítica de processos
- Inteligência artificial
- Blockchain para rastreabilidade
- Análise avançada de dados
Evolução Regulatória:
- Abordagens baseadas em risco
- Testes de liberação em tempo real
- Transformação digital
- Requisitos de sustentabilidade
- Qualidade centrada no paciente
Conclusão
A conformidade com as BPF é essencial para os fabricantes farmacêuticos em Hong Kong. O sucesso requer planejamento abrangente, sistemas robustos, pessoal qualificado e melhoria contínua. As organizações devem se manter atualizadas com as regulamentações em evolução e abraçar os avanços tecnológicos.
Para assistência especializada na implementação e conformidade com as BPF, entre em contato com a ElendiLabs para consulta especializada.
Preços Imbatíveis
Taxas transparentes e competitivas para registro de dispositivos médicos em Hong Kong.
Farmacêutico registrado · Engenheiro de IA · Diretor, ElendiLabs
Farmacêutico registrado, engenheiro de IA, fundador da HKHAIS e especialista em SEO/GEO para o domínio farmacêutico e de dispositivos médicos.
Pergunte Qualquer Coisa
Entraremos em contato pessoalmente.
100% de taxa de resposta • Resposta em até 7 dias úteis
Precisa de Orientação Especializada?
Entre em contato conosco em contact@elendilabs.com / +852 4416 5550