香港醫療儀器科 (MDD) 及醫療儀器行政管理制度 (MDACS) 概覽
衛生署醫療儀器科 (MDD) 及其自願性質的醫療儀器行政管理制度 (MDACS) 簡介,該制度旨在確保香港醫療儀器的安全性、品質及效能。
概覽
此監管機構或司法轄區的要點,及其與市場准入的關係。
簡介
醫療儀器科 (MDD) 隸屬於香港特別行政區政府衛生署,是負責監管醫療儀器安全性、品質及效能的監管機構。
醫療儀器行政管理制度 (MDACS)
MDACS 是目前推行的自願性質行政管理制度,用於規管醫療儀器。其內容包括:
- 儀器表列: 登記第二、三及四級一般醫療儀器,以及 B、C 及 D 級體外診斷醫療儀器。
- 貿易商表列: 登記進口商、分銷商及本地製造商。
- 本地負責人 (LRP): 要求香港境外的製造商委任本地代表,以履行監管義務。
主要職能與角色
- 上市前管制: 根據國際標準(如 ISO 13485)審批表列申請。
- 上市後監察: 建立並管理醫療儀器醫療事故報告及調查系統。
- 資料查詢: 維護表列儀器及貿易商的公開數據庫,以提高透明度。
- 採購標準: 衛生署正逐步規定公立醫療機構使用的儀器必須在 MDACS 表列中(第三階段 Stage C 將於 2026 年 3 月生效)。
粵港澳大灣區 (GBA) 措施
一項特別措施允許大灣區內的指定醫療機構使用香港公立醫院已使用的、具有臨床急需的醫療儀器,促進跨境醫療融合。
文章與指南
ElendiLabs 上標記為此區域的見解文章。
2026年3月20日
ElendiLabs 與 Arqon 比較:全球創新平台與傳統在地代表專長的醫療器械法規服務
ElendiLabs 作為更親民、更具彈性的全球數位平台,擁有更廣泛的國家覆蓋範圍、免費文章附驗證顧問洞見與案例分享,以及透過即時專案配對的更短回應時間;Arqon 則提供可靠的傳統醫療器械諮詢,附在地執照持有、歐盟/美國/亞洲(東南亞)合規支援,以及集團訓練與業務開發服務。ElendiLabs 帶來優越價值、親民價格與可擴展性,實現全球法規成功。
閱讀文章 →
2026年3月19日
ElendiLabs 與 Pacific Bridge Medical 比較:全球創新平台與亞洲傳統專長的醫療器械與藥品法規服務
ElendiLabs 作為更親民、更具彈性的全球數位平台,擁有更廣泛的國家覆蓋範圍、免費文章附驗證顧問洞見與案例分享,以及透過即時專案配對的更短回應時間;Pacific Bridge Medical 則提供可靠的傳統法規與業務開發諮詢,附本地代理代表、臨床試驗,以及專注亞洲的醫療器械、IVD、藥品與生技服務。ElendiLabs 帶來優越價值、親民價格與可擴展性,實現全球法規成功。
閱讀文章 →
2026年3月19日
ElendiLabs 與 Qualtechs 比較:全球創新平台與亞洲傳統專長的醫療器械與藥品法規服務
ElendiLabs 作為更親民、更具彈性的全球數位平台,擁有更廣泛的國家覆蓋範圍、免費文章附驗證顧問洞見與案例分享,以及透過即時專案配對的更短回應時間;Qualtechs 則提供可靠的一站式傳統諮詢與臨床試驗,具深厚亞洲專長。ElendiLabs 帶來優越價值、親民價格與可擴展性,實現全球法規成功。
閱讀文章 →
2026年3月18日
ElendiLabs 與 Asia Actual 比較:全球創新平台與亞洲傳統專長的醫療器械與 IVD 法規服務
ElendiLabs 作為更親民、更具彈性的全球數位平台,擁有更廣泛的國家覆蓋範圍、免費文章附驗證顧問洞見與案例分享,以及透過即時專案配對的更短回應時間;Asia Actual 則提供可靠的本地法規代表與 16 個亞太國家的市場進入支援,具豐富經驗專家。ElendiLabs 帶來優越價值、親民價格與可擴展性,實現全球法規成功。
閱讀文章 →
2026年2月28日
導航亞洲市場藥品註冊
本概述詳細說明香港、台灣以及印尼、馬來西亞、菲律賓、新加坡、泰國和越南等東盟國家的藥品註冊監管框架,包括主要機構、申請程序和市場進入時間表。
閱讀文章 →
2025年12月24日
ISO 13485:2016 解讀:醫療器材品質管理系統實務指南
ISO 13485 是醫療器材產業全球通用的品質管理系統(QMS)標準。本文以實務角度說明其核心要求(文件化、管理責任、設計開發、供應商與生產控制、量測與改善),並提供以風險為本的導入步驟。
閱讀文章 →
2025年12月15日
全球 eCTD 遞交平台:監管專業人士的區域參考指南
電子通用技術文件 (eCTD) 是藥品遞交的全球標準,但每個監管機構都維護其獨特的平台和身份驗證要求。本指南提供了美洲、歐洲、亞太地區和中東主要遞交平台的綜合概覽,並強調了區域模組 1 規範和數位身份驗證方法的重要性。
閱讀文章 →
2025年11月2日
香港批發商牌照(WDL)的作用與要求
香港批發商牌照(WDL)在藥物分銷中的強制性要求概述,包括分銷的廣泛定義、產品註冊職責以及具體的設施和儲存要求,全部以連續敘述形式呈現。
閱讀文章 →
2025年10月27日
香港批發商牌照的要求和職責
在香港獲取和使用批發商牌照(WDL)的詳細法律要求,包括其在藥物註冊中的核心作用以及處理受管制物質(毒藥、危險藥物)的特定要求。
閱讀文章 →
2025年10月22日
進口藥物到香港的注意事項和法律要求
未註冊海外藥物相關風險概述,以及進口藥物作個人用途與商業銷售在香港的法律區別。
閱讀文章 →
2025年10月21日
不良醫藥廣告條例 (UMAO) 第231章:保護公眾免受誤導性聲稱影響
香港的監管工具,用於管制聲稱可預防或治療附表疾病(例如癌症、肺結核)的藥物和療法的廣告,以保障公眾健康免受誇大或虛假聲稱的侵害。
閱讀文章 →
2025年10月20日
香港社區藥房執業指引:從銷售合規到基層醫療和質量保證的轉型
新的《社區藥房執業指引》標誌著香港社區藥房的關鍵轉型,將其角色從單純的配藥(ASP COP)擴展到涵蓋正式的基層醫療服務、風險管理和強制性質量評估。
閱讀文章 →
2025年9月15日
香港中藥補充劑的監管:食物與藥物之間的界限
香港中藥補充劑監管框架的分析,強調了這些產品與註冊專利中成藥 (pCm) 之間的法律區別。
閱讀文章 →
2025年8月21日
香港專利中成藥 (pCm) 註冊:合規與品質標準
香港專利中成藥 (pCm) 強制性註冊流程的全面概述,重點關注三大核心監管支柱:安全、功效和品質 (S.E.Q.)。
閱讀文章 →
2025年7月23日
香港仿製藥物註冊完整指南
了解香港通用藥物(學名藥)的簡略註冊流程,包括生物等效性要求以及成本效益高的藥物所帶來的好處。
閱讀文章 →
2025年6月23日
香港醫療儀器市場准入:監管視角
香港提供了一個充滿活力的醫療儀器市場,擁有獨特的自願上市制度,並正朝著強制性框架過渡。本文根據我們的見解和經驗,涵蓋了監管環境、分類、本地負責人 (LRP) 的關鍵作用,以及為成功進入香港醫療儀器市場而導航的關鍵方面。
閱讀文章 →
2025年6月23日
香港醫療儀器註冊:市場准入之路
香港醫療儀器行政管理制度 (MDACS) 為醫療儀器提供了獨特的自願上市途徑。本文根據我們的見解和經驗,概述了監管框架、本地負責人 (LRP) 的基本作用,以及產品註冊和上市後合規的簡化流程,為高效的香港醫療儀器註冊提供了清晰的途徑。
閱讀文章 →
2025年6月23日
香港醫療儀器註冊:概述
香港醫療儀器行政管理制度 (MDACS) 為醫療儀器和體外診斷儀器提供了自願上市途徑。本文根據我們的見解和經驗,概述了監管環境、分類、本地負責人 (LRP) 的作用以及市場准入的註冊流程,旨在實現高效的香港醫療儀器註冊。
閱讀文章 →
2025年6月23日
香港醫療儀器與體外診斷儀器註冊與批准
香港醫療儀器行政管理制度 (MDACS) 為醫療儀器和體外診斷儀器提供了自願上市途徑,並預計將實施強制性框架。本文根據我們的見解和經驗,探討了分類系統、本地負責人 (LRP) 的關鍵作用以及註冊流程,以促進高效的香港醫療儀器與體外診斷儀器註冊並促進市場准入。
閱讀文章 →
2025年6月23日
香港已上市醫療儀器分銷商作業守則:COP-05 指南
對於香港醫療儀器行政管理制度 (MDACS) 下的已上市醫療儀器分銷商,遵守特定的作業守則對於維持有效的分銷渠道和公共安全至關重要。本文依循 COP-05,詳細闡述了他們在記錄保存、處理和上市後監測等方面的職責,所有這些都來自我們的經驗和見解。
閱讀文章 →
2025年6月23日
香港已上市醫療儀器進口商作業守則:COP-04 指南
對於香港醫療儀器行政管理制度 (MDACS) 下的已上市醫療儀器進口商,遵守特定的作業守則對於確保供應鏈完整性和公共安全至關重要。本文依循 COP-04,詳細闡述了他們在記錄保存、處理和上市後監測等方面的職責,所有這些都來自我們的經驗和見解。
閱讀文章 →
2025年6月23日
香港已上市醫療儀器本地製造商作業守則:COP-03 指南
香港醫療儀器行政管理制度 (MDACS) 下的已上市醫療儀器本地製造商應遵守作業守則,確保質量和安全。本文依循 COP-03,概述了他們在質量管理體系、生產控制和上市後監測方面的職責,所有這些都來自我們的經驗和見解。
閱讀文章 →
2025年6月23日
香港符合性評估機構 (CAB) 作業守則:COP-02 指南
符合性評估機構 (CAB) 在驗證香港醫療儀器行政管理制度 (MDACS) 中醫療儀器合規性方面扮演著至關重要的角色。本文依循作業守則 COP-02,概述了 CAB 的認可流程、職責和運營要求,以確保對醫療儀器安全和性能進行客觀嚴格的評估,所有這些都來自我們的經驗和見解。
閱讀文章 →
2025年6月23日
香港本地負責人 (LRP) 作業守則:COP-01 指南
本地負責人 (LRP) 是香港醫療儀器行政管理制度 (MDACS) 的基石。本文依循作業守則 COP-01,概述了 LRP 在確保醫療儀器在其整個生命週期中的安全、質量和性能方面的廣泛職責和義務,所有這些都來自我們的經驗和知識。
閱讀文章 →
2025年6月23日
香港個性化醫療儀器:TR-009 指南
隨著醫療技術朝向個人化病人護理發展,香港的醫療儀器行政管理制度 (MDACS) 發布了關於個性化醫療儀器的具體指引。本文依循技術參考文件 TR-009,定義並分類了這些儀器——定制、病人匹配和可調適——並闡明了其監管適用性,所有這些都來自我們的經驗和見解。
閱讀文章 →
2025年6月23日
香港人工智能醫療儀器 (AI-MD):TR-008 指南
隨著人工智能改變醫療保健,香港的醫療儀器行政管理制度 (MDACS) 為人工智能醫療儀器 (AI-MDs) 提供了具體指引。本文依循技術參考文件 TR-008,涵蓋 AI-MD 的定義、獨特的監管考量以及必要的文檔要求,包括具有持續學習能力 (CLC) 的 AI-MD,所有這些都來自我們的經驗和見解。
閱讀文章 →

2025年6月23日
香港醫療儀器安全與性能基本原則:深入解讀 TR-004
香港醫療儀器行政管理制度 (MDACS) 的規管基礎建立在安全與性能基本原則之上。本文將特別依循技術參考文件 TR-004,詳細闡述製造商必須將這些基本要求融入儀器生命週期各階段,以確保病人及使用者安全,所有這些都基於我們對穩健香港醫療儀器規管的見解和經驗。
閱讀文章 →
2025年6月23日
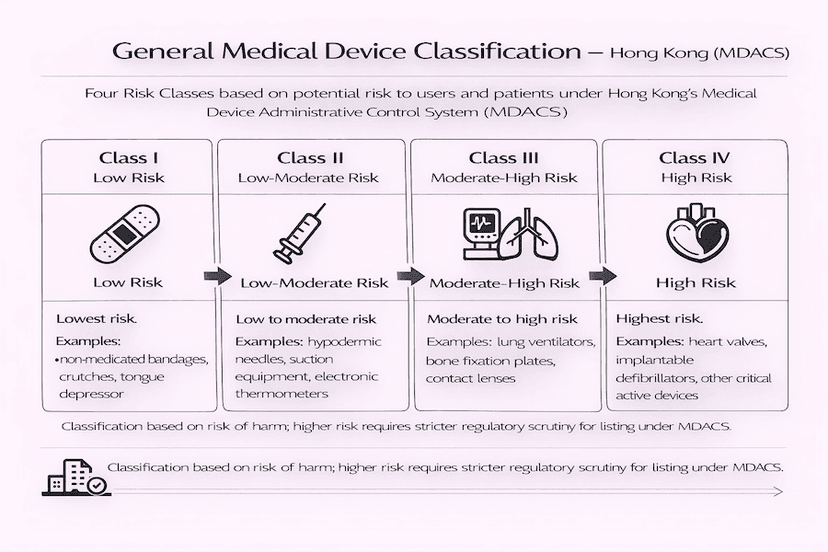
香港通用醫療儀器分類:TR-003 指南
了解通用醫療儀器基於風險的分類對於進入香港市場至關重要。本文依循技術參考文件 TR-003,詳細闡述了在醫療儀器行政管理制度 (MDACS) 下確定儀器風險類別的規則和因素,所有這些都基於我們對高效香港醫療儀器分類的見解和經驗。
閱讀文章 →

2025年6月23日
香港醫療儀器摘要技術文件 (STED):TR-002 指南
摘要技術文件 (STED) 是香港醫療儀器行政管理制度 (MDACS) 下醫療儀器上市申請的關鍵組成部分。本文依循技術參考文件 TR-002,解釋 STED 的目的和所需內容,以證明符合安全和性能基本原則,所有這些都基於我們對簡化香港醫療儀器文件流程的見解和經驗。
閱讀文章 →
2025年6月23日
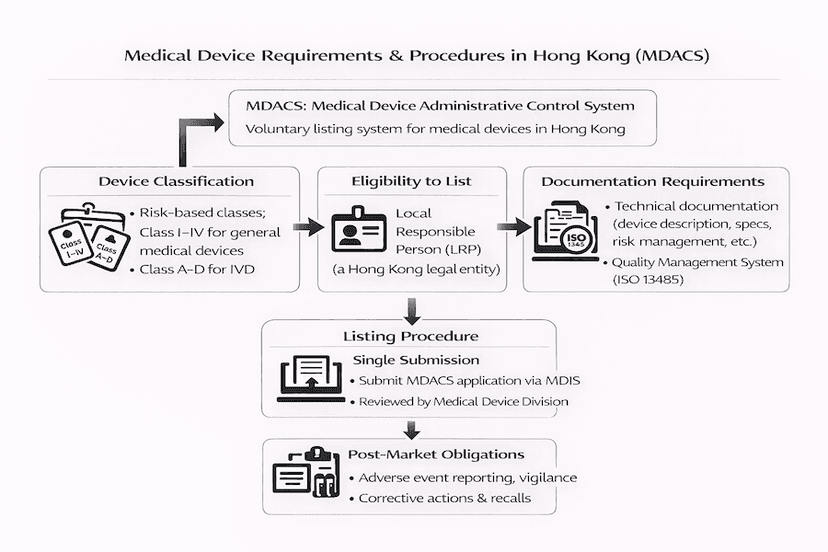
香港醫療儀器註冊:基本要求和程序
本指南基於我們的見解和經驗,提供有關香港醫療儀器行政管理制度(MDACS)下醫療儀器註冊的基本要求和程序的全面指南,以實現高效的香港醫療儀器註冊。
閱讀文章 →
2025年6月16日
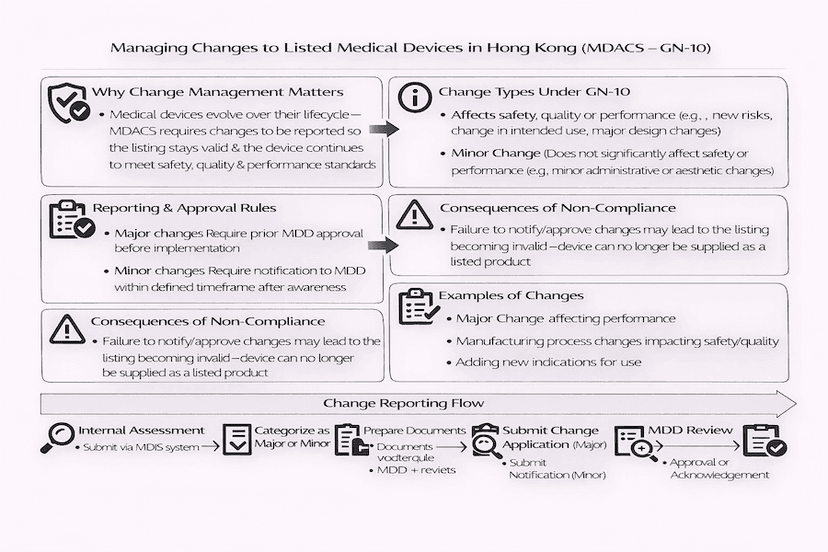
香港已上市醫療儀器變更管理:GN-10 指南
根據香港醫療儀器行政管理制度 (MDACS) 的已上市醫療儀器變更需要仔細管理和呈報。本文依循 GN-10 指南,基於我們的見解,解釋本地負責人 (LRP) 應如何分類、管理和呈報主要及次要變更,以確保持續合規和病人安全。
閱讀文章 →
2025年6月16日
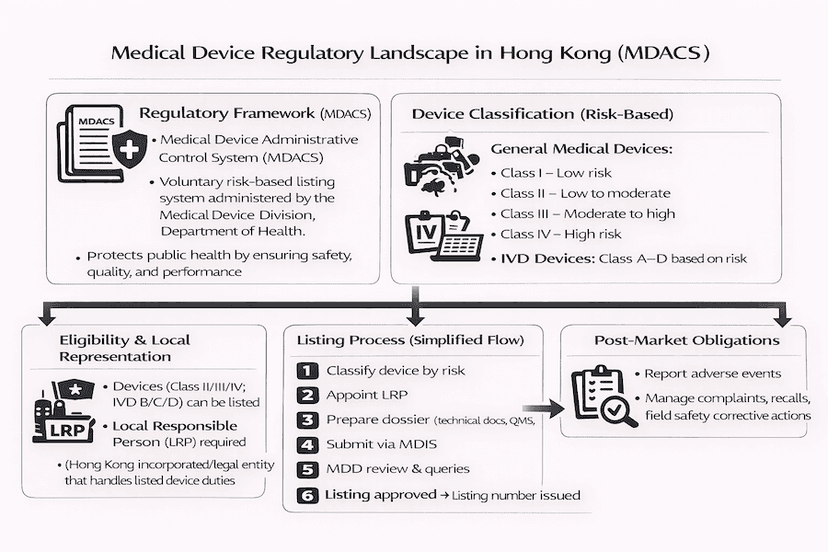
香港醫療儀器監管環境導航
從我們的見解和經驗出發,詳細概述香港醫療儀器行政管理制度 (MDACS),涵蓋儀器分類、全面的表列程序、上市後責任以及未來強制性監管的前景。
閱讀文章 →
2025年6月15日
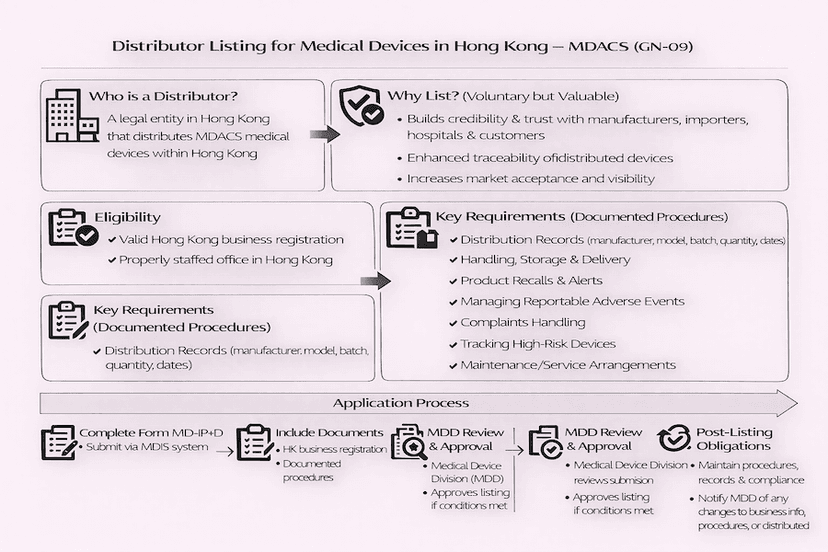
香港醫療儀器分銷商上市程序:GN-09 指南
本文概述了醫療儀器分銷商根據香港醫療儀器行政管理制度 (MDACS) (依循 GN-09 指引) 申請上市的程序。內容涵蓋申請資格、文件化程序的主要要求以及提交流程,旨在加強可追溯性和公共安全,這都是基於我們的見解。
閱讀文章 →
2025年6月14日
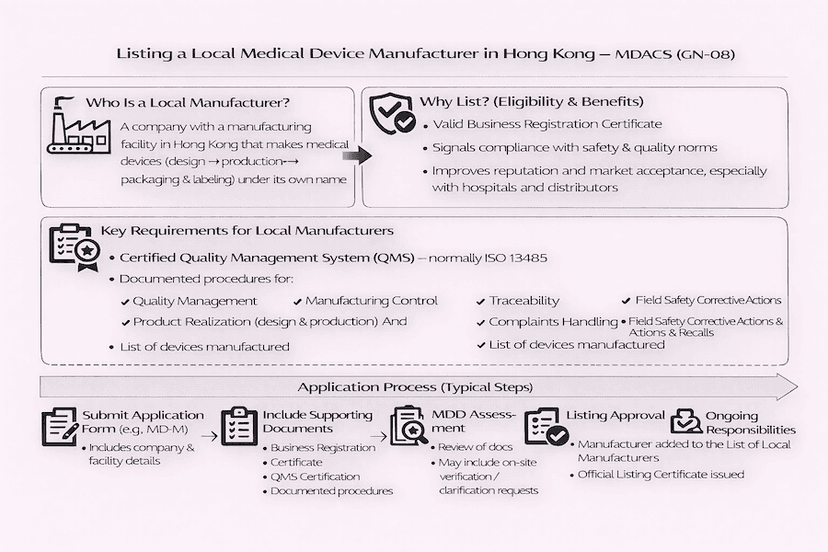
香港醫療儀器本地製造商上市程序:GN-08 指南
本文詳細闡述了香港醫療儀器本地製造商根據醫療儀器行政管理制度 (MDACS) (依循 GN-08 指引) 申請上市的程序。內容涵蓋申請資格、質量管理體系要求以及提交流程,所有這些都基於我們對高效香港醫療儀器製造的見解和經驗。
閱讀文章 →
2025年6月14日
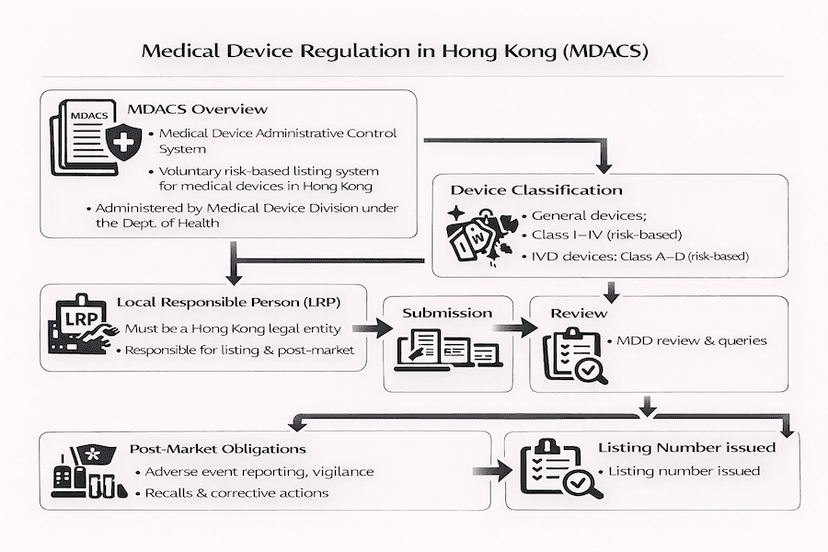
深入了解香港醫療儀器規管:MDACS 框架
香港的醫療儀器行政管理制度 (MDACS) 為醫療儀器規管提供了一個健全但目前屬自願性質的框架。本文將深入探討該制度的主要特點,包括儀器分類、上市程序、本地負責人 (LRP) 的關鍵作用,以及其對市場准入和公共採購日益增長的重要性,所有這些都來自我們的見解和經驗。
閱讀文章 →
2025年6月2日
香港乙、丙、丁類體外診斷醫療儀器上市程序:GN-06 指南
本文詳細闡述了根據香港醫療儀器行政管理制度 (MDACS) (依循 GN-06 指引) 申請將乙、丙、丁類體外診斷醫療儀器 (IVDMDs) 上市的程序。內容涵蓋分類、申請資格、提交要求以及透過MDIS在線申請,所有這些都基於我們對高效香港 IVDMD 上市的見解和經驗。
閱讀文章 →
2025年6月1日
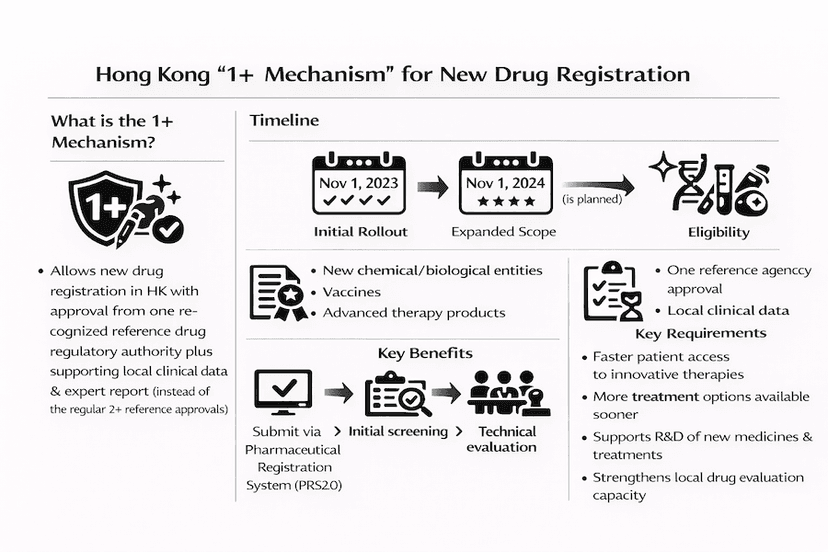
"1+"機制:加速香港新藥註冊
透過我們的見解與經驗,了解香港創新的"1+"藥物註冊機制,其對患者獲得新治療的影響,以及在促進大灣區醫療保健發展中的作用。
閱讀文章 →

2025年5月24日
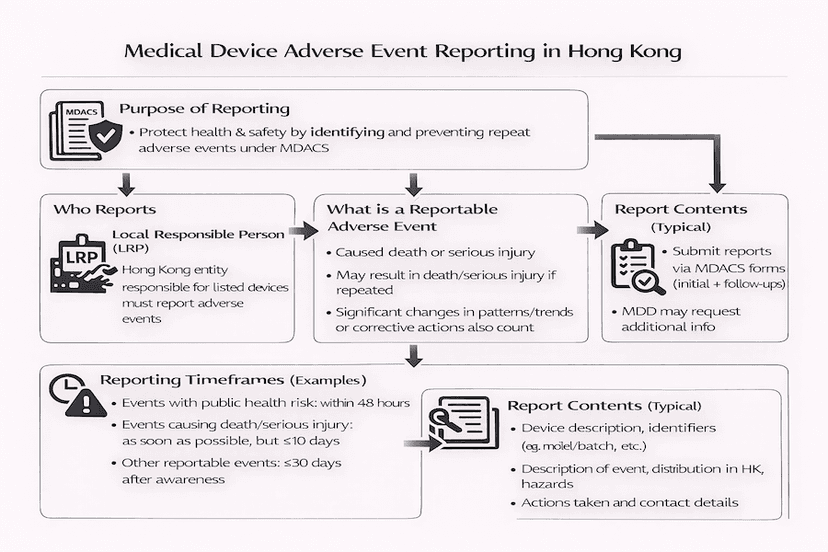
香港醫療儀器不良事件呈報:本地負責人 (LRP) 指南
不良事件呈報是香港醫療儀器行政管理制度 (MDACS) 的關鍵組成部分,旨在加強公共衛生和安全。本文根據我們的見解,概述了本地負責人 (LRP) 在呈報已上市醫療儀器相關不良事件方面的要求和職責。
閱讀文章 →
2025年5月17日
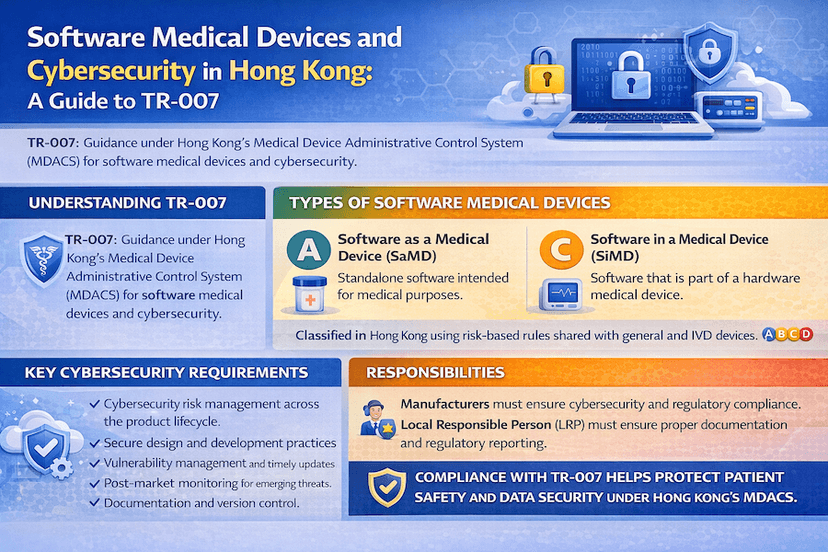
香港醫療儀器軟件與網絡安全:TR-007 指南
隨著軟件在醫療保健中扮演日益重要的角色,香港的醫療儀器行政管理制度 (MDACS) 正在解決其監管問題,包括網絡安全。本文依循技術參考文件 TR-007,概述了醫療儀器軟件 (SaMD) 和醫療儀器中軟件 (SiMD) 的定義,以及製造商和 LRP 必須考量的重要網絡安全因素,所有這些都基於我們對穩健香港醫療儀器網絡安全的見解和經驗。
閱讀文章 →
2025年5月10日
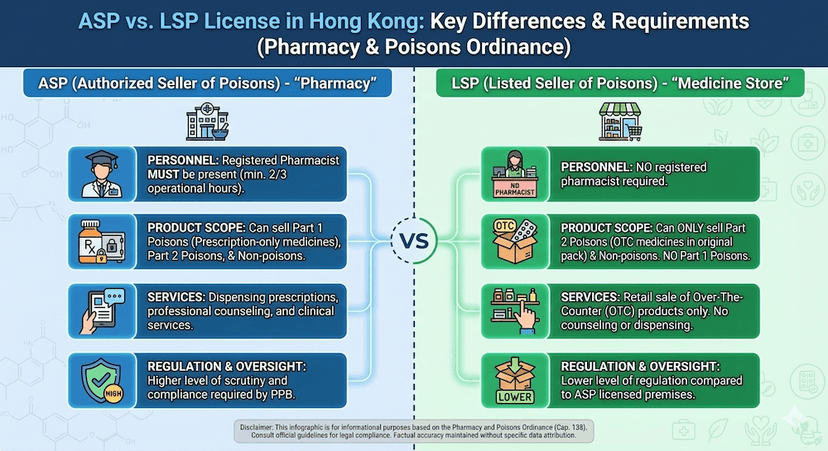
ASP 與 LSP 牌照:您需要哪一種?
了解 Authorized Seller of Poisons (ASP) 註冊毒藥銷售商和 Listed Seller of Poisons (LSP) 表列毒藥銷售商牌照之間的區別,並確定哪種適合您的業務需求和營運模式。
閱讀文章 →
2025年5月3日
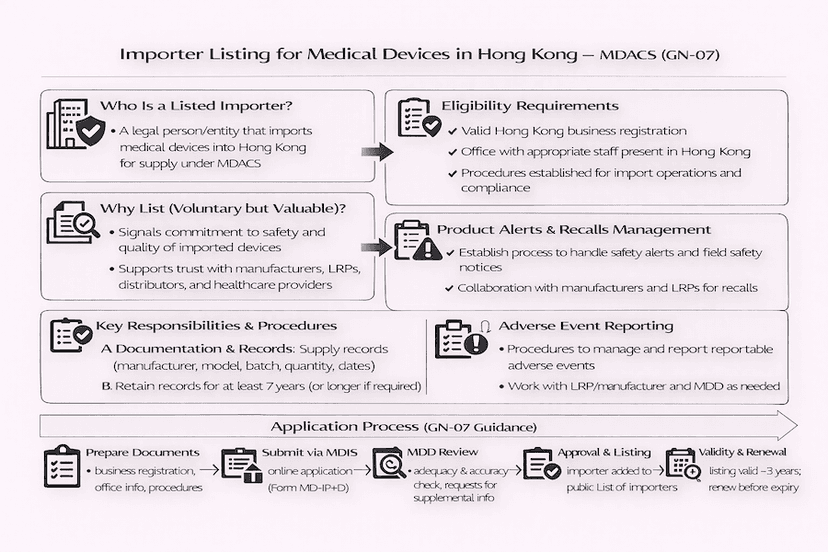
香港醫療儀器進口商上市程序:GN-07 指南
對於將醫療儀器進口至香港的實體,醫療儀器行政管理制度 (MDACS) 提供了一項進口商自願上市計劃,依循 GN-07 指引。本文根據我們的見解和經驗,詳細闡述了作為醫療儀器進口商上市的資格、申請步驟和主要要求,以實現高效的香港醫療儀器進口。
閱讀文章 →
2025年4月18日
香港醫療儀器註冊:市場與監管概覽
香港為醫療儀器提供了不斷增長且充滿活力的市場,並受醫療儀器行政管理制度 (MDACS) 管轄。本文根據我們的見解和經驗,概述了該地區的監管環境、主要市場趨勢、儀器分類以及註冊和市場准入的一般流程。
閱讀文章 →
2025年4月17日
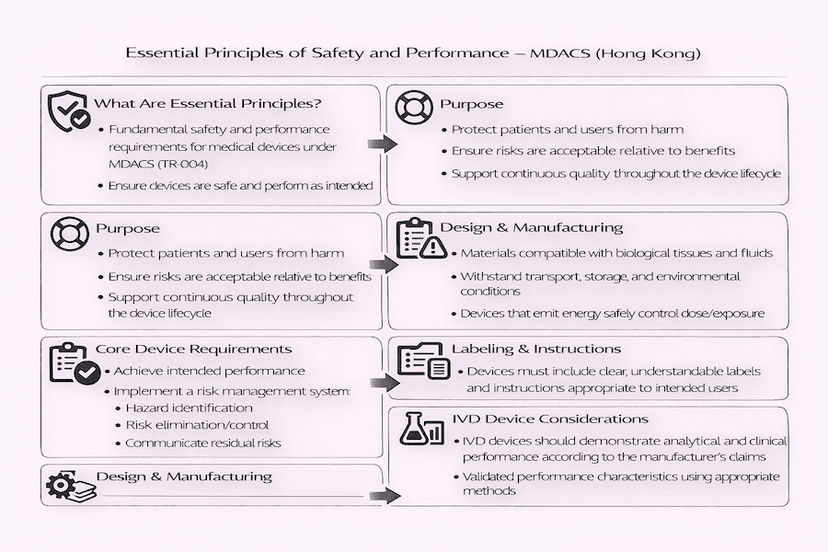
香港醫療儀器安全與性能基本原則:理解 TR-001 和 TR-004
香港醫療儀器的安全和性能基於一套「基本原則」,詳載於醫療儀器行政管理制度 (MDACS) 的技術參考文件 TR-001 和 TR-004 中。本文根據我們的見解和經驗,探討了製造商在醫療儀器設計、製造和上市後階段必須滿足的這些基本要求,旨在實現穩健的香港醫療儀器監管。
閱讀文章 →
2025年4月12日
香港醫療儀器產品註冊:聚焦方法
應對香港醫療儀器監管合規性對於市場准入至關重要。本文重點介紹了為醫療儀器行政管理制度 (MDACS) 準備產品以及簡化註冊流程以實現高效市場准入的服務,這都是基於我們的見解。
閱讀文章 →
2025年4月6日
全球醫療器材註冊:主要市場的監管期望
將單一醫療器材引入多個市場需要了解不同的監管期望,這絕非「複製貼上」那麼簡單。主要差異包括歐盟對臨床證據的關注 (MDR)、美國對實質等效性的依賴 (510(k)),以及日本高度程序驅動的審查,強調了穩健的全球策略和利用像 **MDSAP** 等計劃的潛力。
閱讀文章 →
2025年3月21日
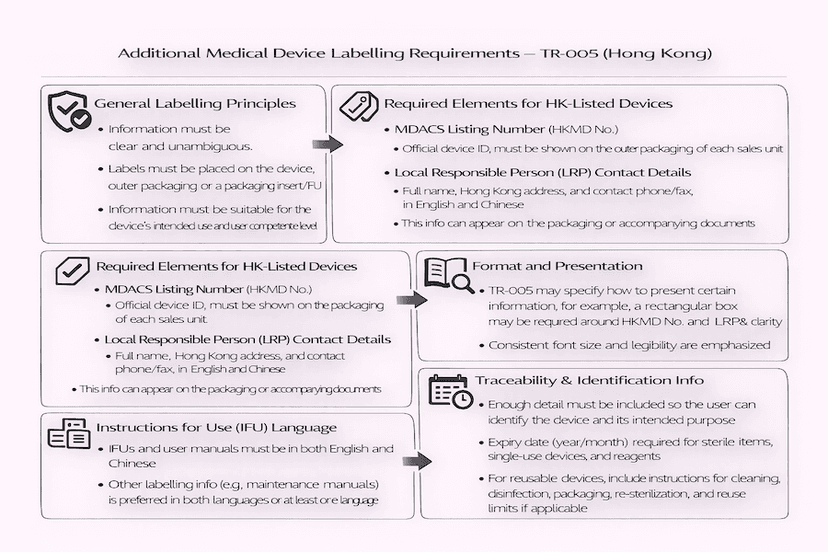
香港醫療儀器額外標籤要求:理解 TR-005
除了通用基本原則外,香港的醫療儀器行政管理制度 (MDACS) 對醫療儀器施加了特定的額外標籤要求。本文依循技術參考文件 TR-005,詳細闡述了這些關鍵要素,以確保在本地市場上清晰的溝通和合規性,所有這些都基於我們對高效香港醫療儀器標籤的見解和經驗。
閱讀文章 →
2025年3月17日
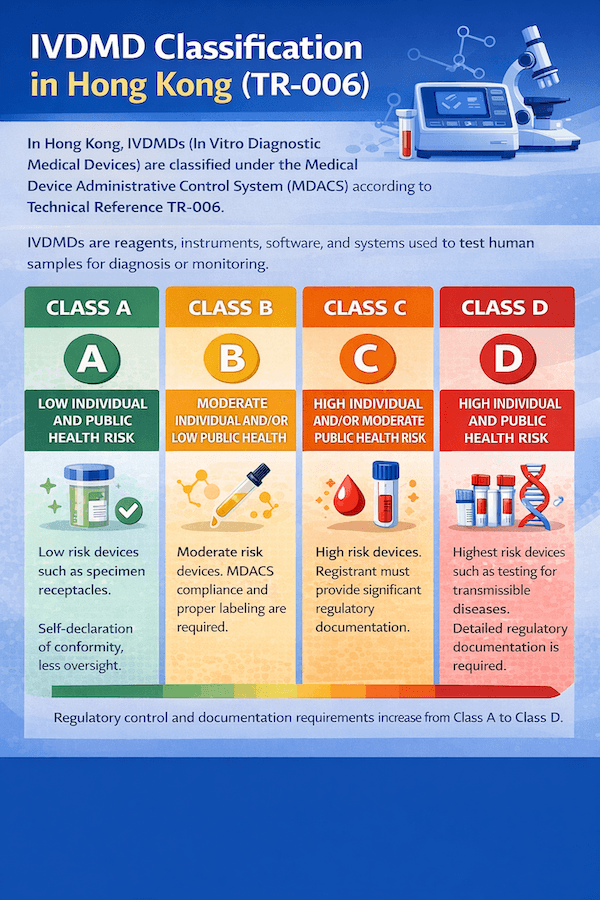
香港體外診斷醫療儀器 (IVDMDs) 分類:TR-006 指南
香港體外診斷醫療儀器 (IVDMDs) 的分類是一個基於風險的系統,對於符合監管規定至關重要。本文依循技術參考文件 TR-006,概述了在醫療儀器行政管理制度 (MDACS) 下確定 IVDMD 風險類別的原則和類別,所有這些都基於我們對高效香港 IVDMD 分類的見解和經驗。
閱讀文章 →
2025年3月5日
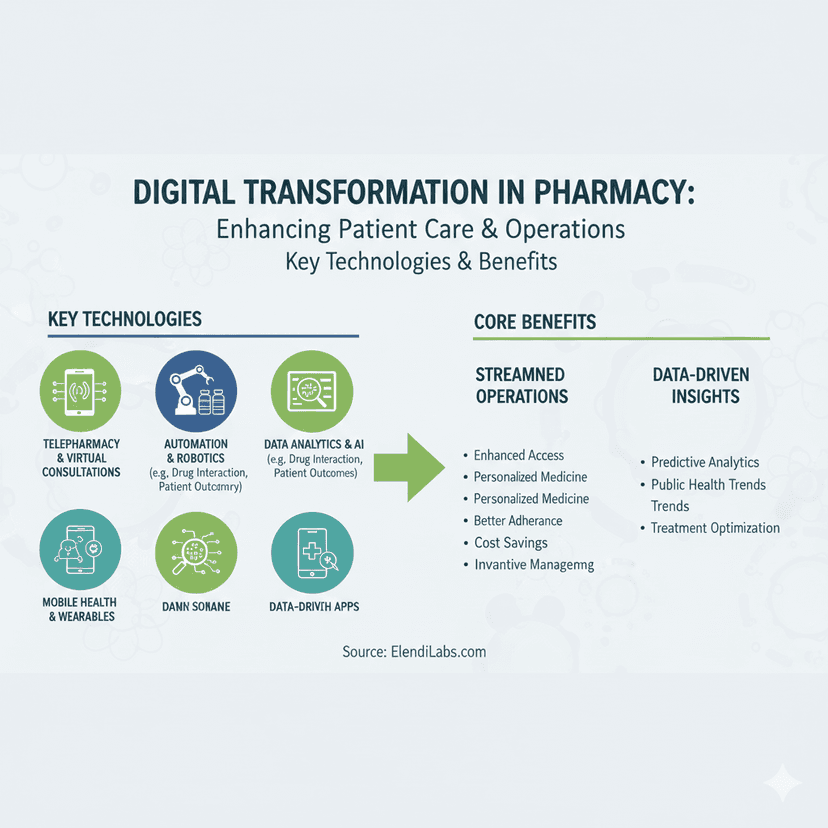
藥房管理的數碼轉型 (Digital Transformation)
現代軟件解決方案如何在數碼時代徹底改變藥房營運、提高效率並改善病人護理。深入探討 Pharmacy Management Systems (PMS)、人工智能 (AI) 和機器學習 (Machine Learning) 的應用。
閱讀文章 →

2025年1月28日
香港的藥物警戒最佳實踐 (Pharmacovigilance Best Practices)
香港藥業中不良事件報告和藥物警戒合規的重要指引。涵蓋 Adverse Event Reporting、Safety Signal Detection 和 Risk Management Plans (RMP) 的實施要點。
閱讀文章 →
2025年1月16日
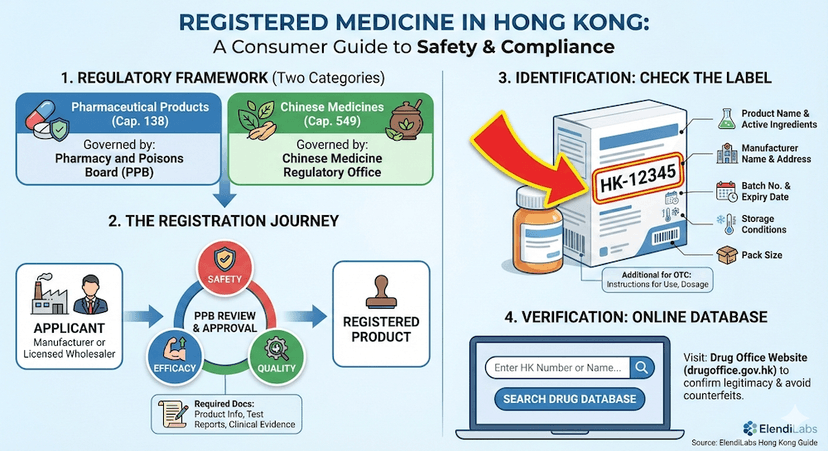
了解香港註冊藥物:完整指南
了解香港的藥物註冊系統、法律要求以及如何識別註冊藥物以確保安全性和有效性。涵蓋藥劑業及毒藥管理局的註冊程序和消費者保護措施。
閱讀文章 →
2025年1月15日
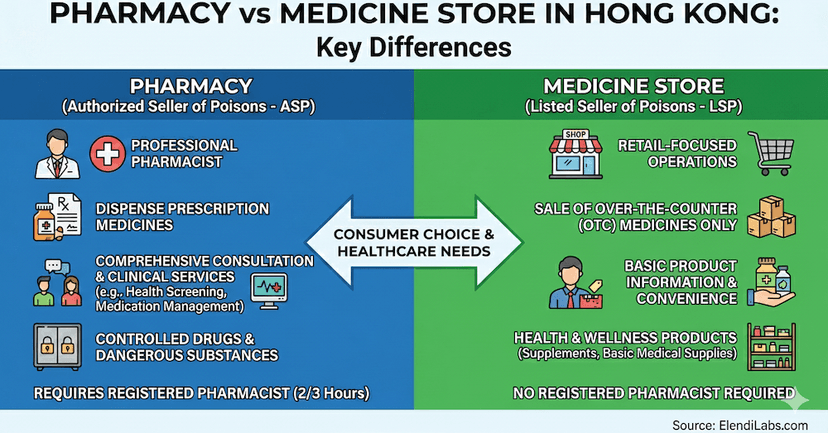
藥房與藥行:了解主要差異
「藥房」設有註冊藥劑師配發處方藥物,而「藥行」主要售賣非處方成藥。立即在此了解兩者在法律規管及服務上的關鍵區別。
閱讀文章 →

2024年12月20日
藥品進出口法規 (Import and Export Regulations)
通過這份詳細指南,了解香港複雜的藥品進出口法規環境。包括 Import License (Form 3)、Export License (Form 6) 和 Wholesale Dealer License (WDL) 的申請程序。
閱讀文章 →
2024年10月15日
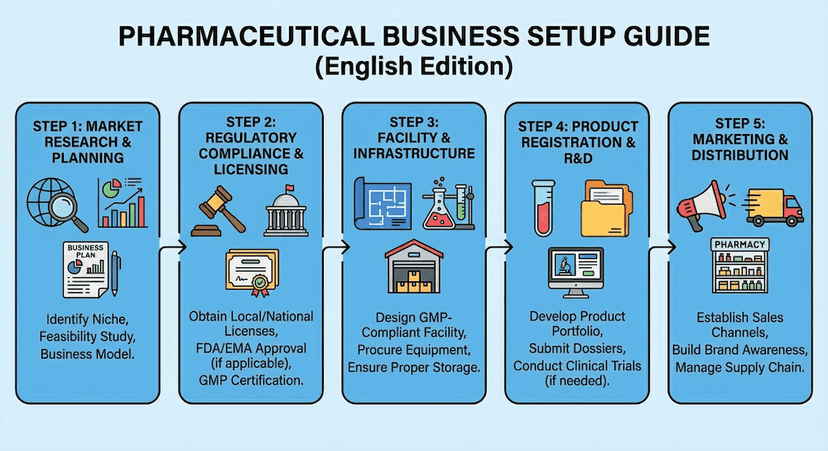
在香港設立您的藥業企業 (Pharmaceutical Business Setup)
在香港建立藥業企業的逐步指南,從牌照申請到營運要求。涵蓋 Good Manufacturing Practice (GMP)、Good Distribution Practice (GDP) 和各種牌照的申請流程。
閱讀文章 →
2024年8月10日
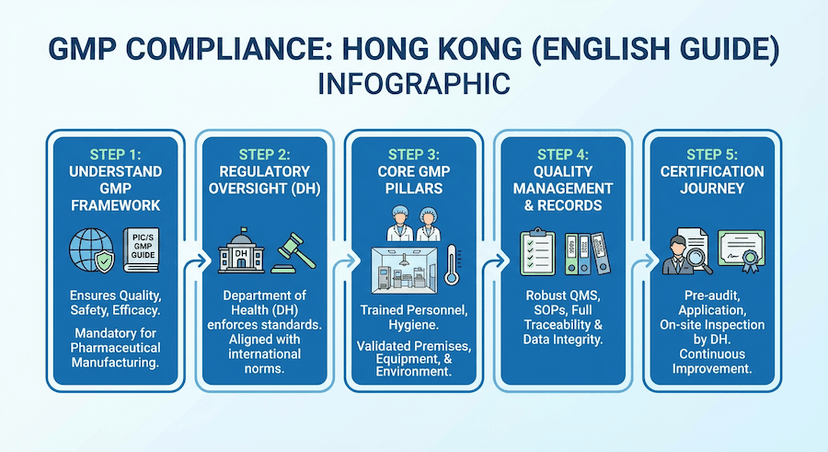
香港的良好製造規範 (GMP) 合規
在藥品製造設施中實施 GMP 合規的基本要求和最佳實踐。涵蓋設施設計、質量管理系統、驗證程序和監管檢查準備。
閱讀文章 →
2024年7月20日
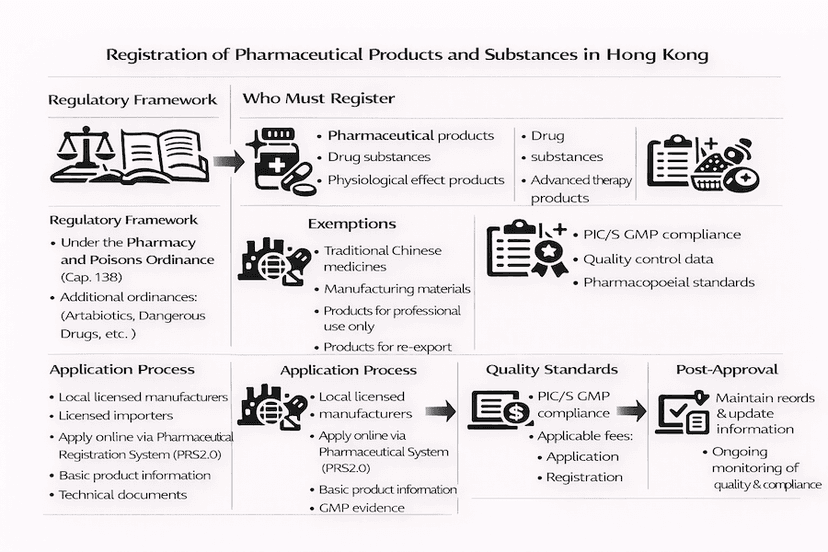
專業指南:香港藥劑製品註冊
為醫療專業人員和行業利益相關者提供的香港藥品和物質註冊要求、程序和合規性的全面指南。
閱讀文章 →
2024年6月5日
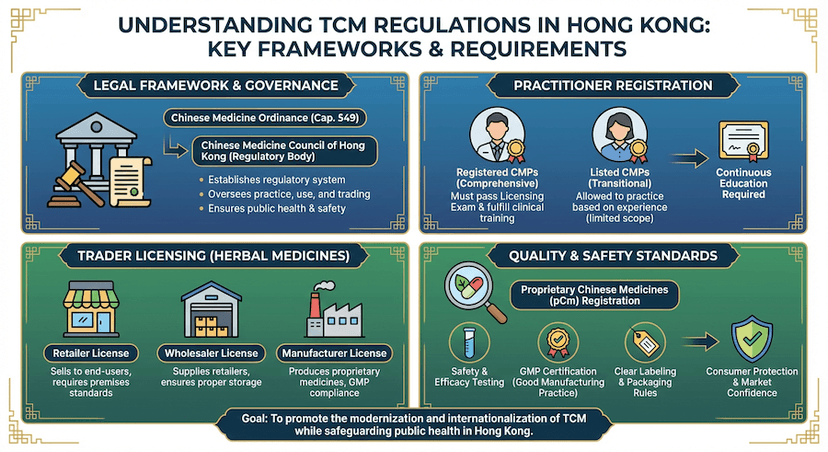
香港的中醫藥法規 (Traditional Chinese Medicine Regulations)
中醫藥法規的全面指南,包括執業者註冊和中藥牌照。涵蓋中成藥註冊、中藥材貿易和質量標準要求。
閱讀文章 →
2024年5月10日
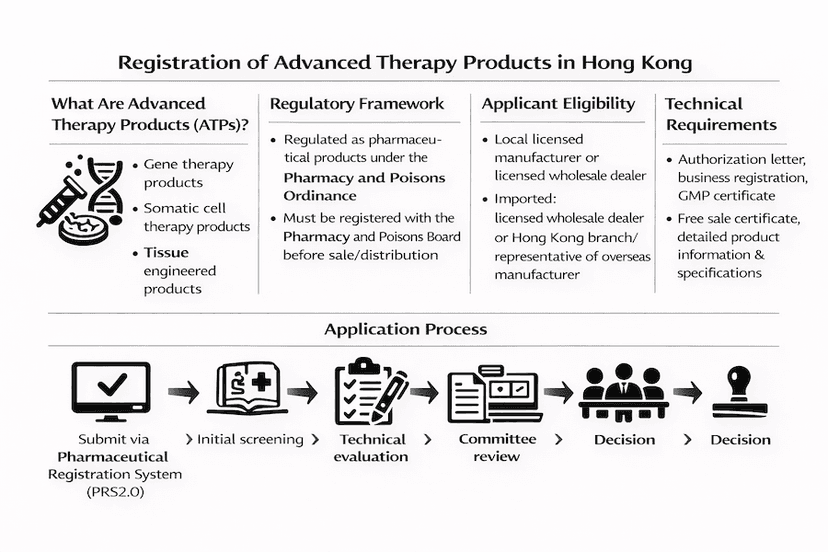
香港先進治療產品註冊:完整指南
了解香港先進治療產品(ATPs)的註冊程序,包括基因治療、體細胞治療和組織工程產品。
閱讀文章 →
2024年3月20日
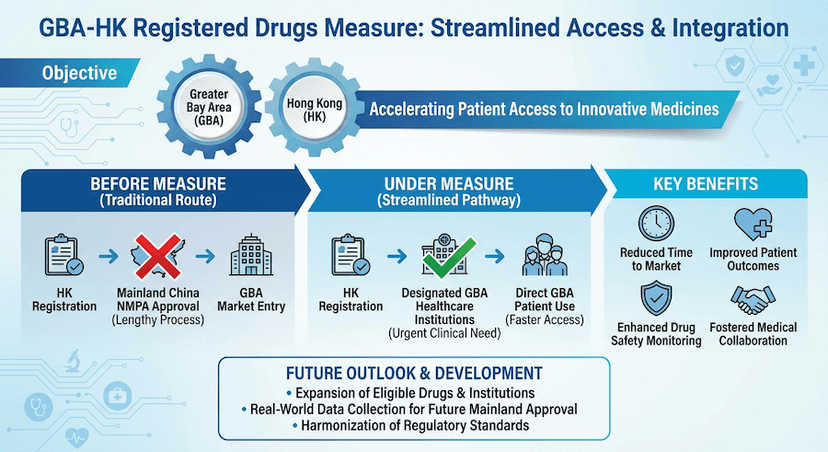
在大灣區使用香港註冊藥物和醫療器械:全面指南
了解允許大灣區指定醫療機構使用香港註冊藥物和醫療器械的創新措施,為香港居民提供更好的醫療服務。
閱讀文章 →
2024年3月20日
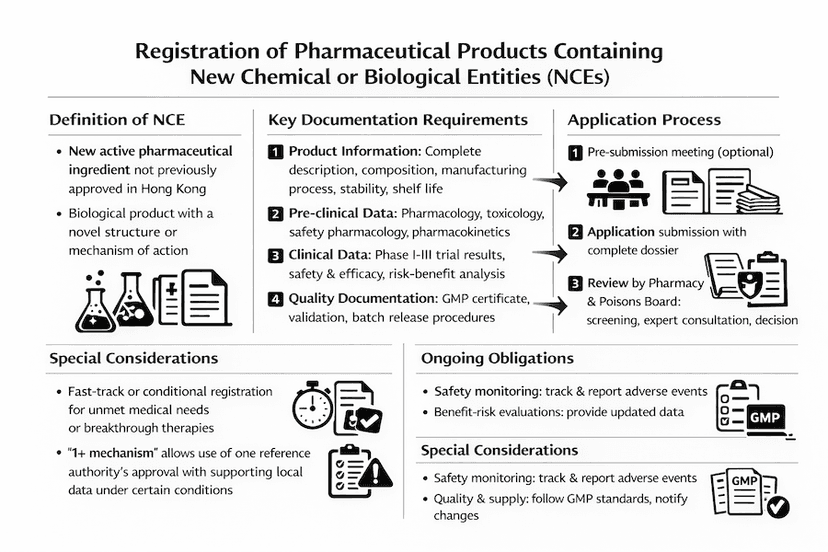
香港含新化學或生物實體的藥劑製品註冊
香港含新化學或生物實體的藥劑製品註冊的完整指南,包括要求、程序和監管考慮因素。
閱讀文章 →
2024年2月20日
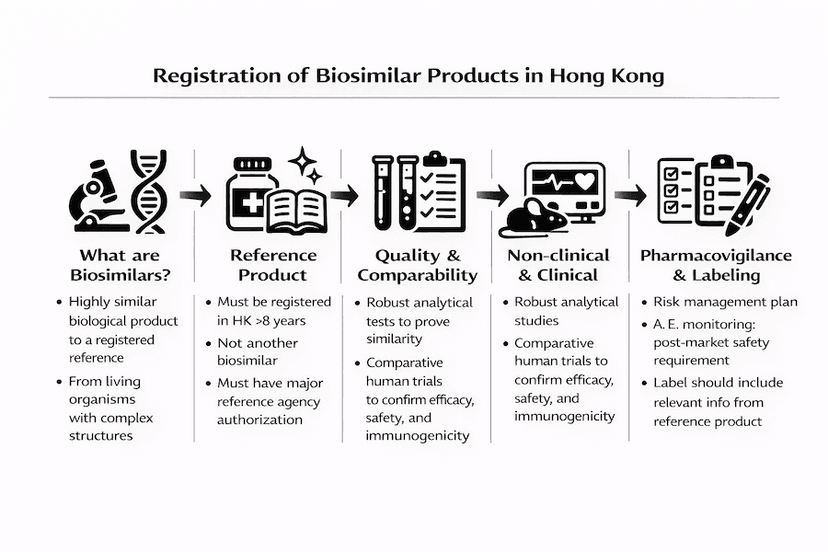
香港生物類似藥註冊:完整指南
了解香港生物類似藥的註冊程序,包括要求、文件以及這些複雜生物藥物的特殊考慮因素。
閱讀文章 →